0 9 промилле алкоголя это сколько: Нормы алкоголя в крови. Что такое промилле и как рассчитать его самостоятельно
перевод промилле в мг л
Для автомобилистов, которые «по праздникам» употребляют спиртные напитки, чрезвычайно актуальным является вопрос проверки на алкоголь сотрудниками ГИБДД. Этот вопрос стал еще более актуальным после изменения правил о максимальном возможном показателе этанола в крови. Многие автомобилисты считают, что если существует предельно разрешенный показатель, то значит, они имеют право употребить небольшой объем спиртосодержащих напитков перед поездкой.
Однако перед тем, как определить допустимый объем употребленного спирта, нужно разобраться с общепринятым обозначением этого показателя. Напомним, проверка водителя на содержание спиртосодержащих напитков в крови выполняется в промилле. Для перевода промилле в мг л нужно четко осознавать суть данного понятия.
Что обозначает промилле?
Под обозначением «промилле» подразумевается тысячная доля. Применение этого термина обусловлено тем, что для измерения добавочных взвесей, содержащихся в жидкости, чрезвычайно неудобно использовать проценты.
Эта единица измерения нужна для выявления концентрации спиртосодержащих жидкостей в крови. Необходимо заметить, что промилле имеет один любопытный нюанс, касающийся разницы между полами. У женщин промилле накапливаются на порядок быстрее, чем у мужчин.
Как определяется промилле?
Подсчеты в тысячных долях практически не отличаются от математических операций в процентах. Промилле принято обозначать знаком ‰. Данный значок очень напоминает всем известный процент «%», однако между этими обозначениями есть значительная разница. В процессе определения дозы этанола
- 10‰ = 1% = 10/1000 = 0,01;
- 1500‰ = 150% = 1500/1000 = 1,50;
- 250‰ = 25% = 250/1000 = 0,25;
- 450‰ = 45% = 450/1000 = 0,45;
- 0,20‰ = 0,02% = 0,2/1000 = 0,0002.

Как показывает этот пример, перевод промилле в проценты и обратно не слишком принципиален. Здесь нужно понимать исключительно базовые соотношения.
Знание соотношений позволяет без проблем получить данные, требуемые для расчета дозировки употребленных алкогольных напитков, уровня спирта в крови и времени, необходимого для расщепления метаболитов.
Для выполнения большего количества расчетов, необходимо знать несколько важнейших параметров:
- возраст;
- пол;
- вес;
- текущее состояние здоровья;
- психологическое состояние;
- тип выпитого спиртосодержащего напитка.
Как необходимо рассчитывать промилле
Для понимания того, как правильно выполнить расчет промилле, необходимо рассмотреть конкретный пример. Предположим, что некий мужчина весом 90 кг выпил 0,3 л водки крепостью в 40%. Измерение промилле будет выполнено по такому алгоритму:
- Расчет массы жидкости в организме.
 Здесь необходимо вспомнить школьную программу обучения. Напомним, что в организме мужчины содержится 70% жидкости. Следовательно, масса жидкости равна 63 кг.
Здесь необходимо вспомнить школьную программу обучения. Напомним, что в организме мужчины содержится 70% жидкости. Следовательно, масса жидкости равна 63 кг. - Определение дозировки этанола. Для этого нужно умножить объем употребленного спиртного напитка на его крепость: 300 мл х 40% = 120 мл. Если делать расчеты в граммах, то это показатель будет равен 120 мл х 0,79 (плотность этанола) = 94,8 г. Следовательно, содержание в крови этанола крепостью 100% составит 94,8 – 10% = 85,32 грамма.
- Резюмируя, необходимо сказать, что итоговая концентрация спирта в крови этого мужчины будет равна: 85,32 г: 63 кг = 1,35 промилле.
Этот пример демонстрирует, что без проблем определить показатель промилле может любой желающий. Для этого достаточно использовать указанные формулы и выполнять примитивные математические операции. Тем не менее, следует акцентировать внимание на том, что указанный пример является довольно-таки условным, а не абсолютным. Это обусловлено тем, что спиртные напитки употребляются не одним махом, а постепенно. Следовательно, с момента первого приема напитка этанол постепенно выводиться из организма. Также стоит помнить и о приведенных выше дополнительных параметрах, которые позволяют определить точное содержание алкоголя в плазме крови.
Это обусловлено тем, что спиртные напитки употребляются не одним махом, а постепенно. Следовательно, с момента первого приема напитка этанол постепенно выводиться из организма. Также стоит помнить и о приведенных выше дополнительных параметрах, которые позволяют определить точное содержание алкоголя в плазме крови.
Измерение алкотестером
Сегодня совершенно необязательно использовать формулы для определения уровня опьянения. Теперь для этих нужд можно использовать вполне доступный прибор под названием алкотестер. Этот прибор предназначен для анализа воздуха, выдыхаемого человеком.
Стоит сказать, что в большинстве стран ЕС действует закон, который предписывает автомобилистам всегда иметь при себе алкотестер. Благодаря этому, водители смогут самостоятельно принимать решение о возможности сесть за руль после «гулянки».
Учитывая, что алкотестеры показывают результаты в тысячных долях, а в законе максимально допустимый уровень этилового спирта в крови указан в мг/л, у многих водителей возникают сложности с тем, как перевести мг л в промилле.
Соотношение м/г и промилле
Согласно действующему законодательству, максимально допустимая доза спиртосодержащих напитков в крови водителя составляет 0,16 мг/л. Это означает, что предельно разрешенный показатель промилле в воздухе, который выдыхает автомобилист, равен 0,34‰. Если алкотестер показывает более высокий результат, водитель понесет административную ответственность за вождение в нетрезвом виде.
Для понимания соответствия и разницы между миллиграммами и промилле используется специальная таблица перевода промилле в мг л. Эта таблица предусматривает несколько состояний:
- Норма – до 0,3 ‰ или до 0,135 мг/л в потоке воздуха.
- «Подпитие» — до 0,9 ‰ или до 0,405 мг/л в потоке воздуха.
- Первичная степень опьянения – до 1,9 ‰ или до 0,855 мг/л в потоке воздуха.
- Вторая степень опьянения – до 2,9 ‰ или до 1,305 мг/л в потоке воздуха.
- Тяжелая стадия опьянения – до 3,9 ‰ или до 1,755 мг/л в потоке воздуха.

- Алкогольная кома – от 4 ‰ и от 1,8 мг/л в потоке воздуха.
Стадии опьянения
Наркологи выделяют 3 основных стадии опьянения. Если на первой стадии наличие алкогольного опьянения едва определяется, то третий уровень пьяности может привести к летальному исходу. Таким образом, фраза «допиться до смерти» вполне правдива. Это может произойти в том случае, если в организме взрослого здорового человека скапливается более 4 грамм чистого этанола на килограмм тела. Для пожилых людей и лиц, страдающих от каких-либо заболеваний, критичным уровнем чистого этанола является 3 грамма.
Если сделать перевод мг в промилле, то наблюдается следующая картина:
- 0,5-1,5‰ – первичная стадия;
- 1,5-2,5‰ – вторая стадия;
- 2,5-3‰ – тяжелая степень;
- 3-5‰ – крайне тяжелая степень;
- 5-6‰ – смертельная дозировка этанола.
Какие могут быть последствия езды в нетрезвом виде
Перед тем, как переводить мг л в промилле и посчитать сколько можно выпить спиртосодержащих напитков, нужно помнить, что идеальным водителем может быть исключительно трезвый человек.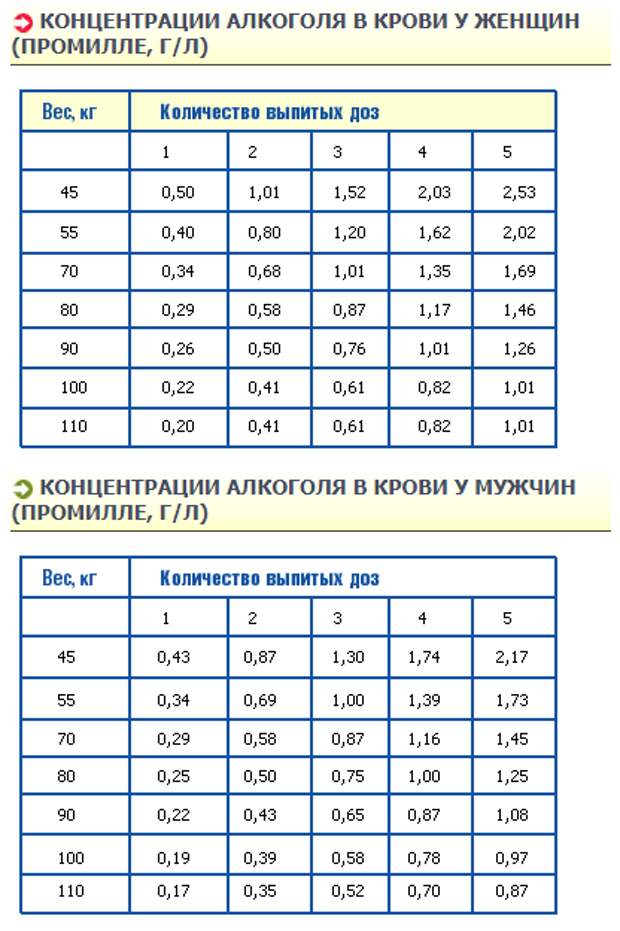 Но в жизни случаются разные ситуации, и вопрос измерения промилле всегда будет актуальным.
Но в жизни случаются разные ситуации, и вопрос измерения промилле всегда будет актуальным.
И все-таки нужно понимать, что алкоголь негативно сказывается на реакции автомобилиста. И это влияние напрямую зависит от показателя этанола в крови. Например, при минимальном уровне водитель уже не способен адекватно оценивать дорожную ситуацию. У человека с незначительным опьянением
Начальная стадия не позволяет автомобилисту адекватно оценивать расстояния до объектов на дороге. Также наблюдается неправильное восприятие света и сигналов светофора. Наконец, средний уровень характеризуется неспособностью управлять автомобилем и существенным нарушением зрения. Автомобилист в таком состоянии не способен адекватно воспринимать действительность.
Выводы
Резюмируя, нужно сказать, что любой водитель должен нести ответственность и оставаться полностью трезвым.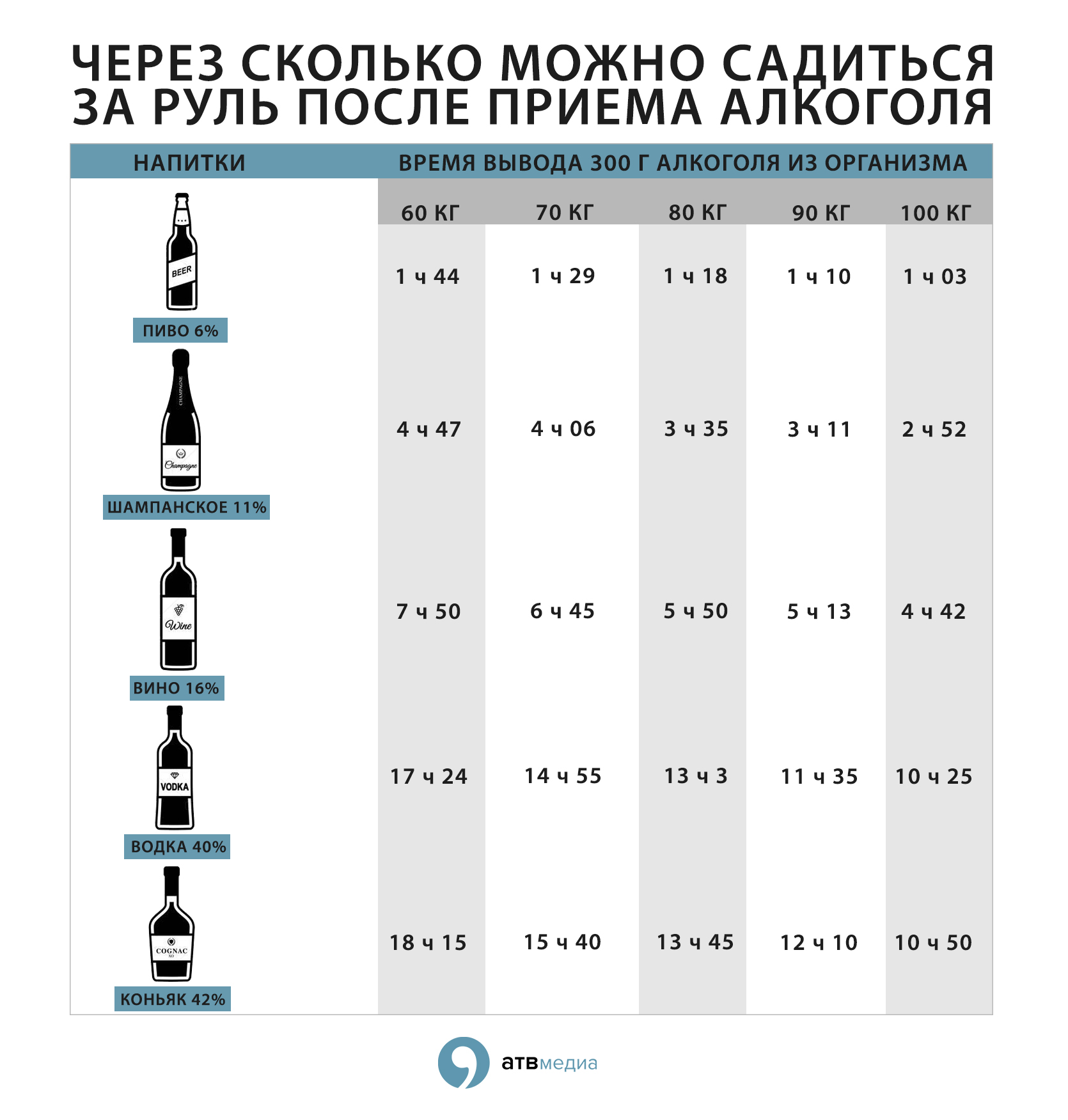 В этом случае возможность возникновения аварийной ситуации сводится к нулю. Поэтому перед тем, как начать переводить алкоголь из мг в промилле, нужно помнить, что вы несете ответственность не только за себя, но и за своих пассажиров. К тому же не стоит рисковать жизнью других участников дорожного движения.
В этом случае возможность возникновения аварийной ситуации сводится к нулю. Поэтому перед тем, как начать переводить алкоголь из мг в промилле, нужно помнить, что вы несете ответственность не только за себя, но и за своих пассажиров. К тому же не стоит рисковать жизнью других участников дорожного движения.
Установлен новый рекорд по содержанию алкоголя в крови :: Общество :: РБК
 Концентрация же в 5 промилле обычно является смертельной.
Концентрация же в 5 промилле обычно является смертельной.Житель болгарского города Пловдив по фамилии Петров побил европейский рекорд по уровню алкоголя в крови, улучшив его почти на 2 промилле, сообщает радиостанция «Эхо Москвы». В ходе обследования медики установили, что в крови 67-летнего пациента было 9,14 промилле алкоголя. Концентрация же в 5 промилле обычно является смертельной.
Причем пожилой любитель спиртного оказался на больничной койке случайно. Туда он попал не из-за алкогольного отравления, а после того как его сбил автомобиль. Сделав анализы, медики не поверили своим глазам и повторили исследование 5 раз.
Сделав анализы, медики не поверили своим глазам и повторили исследование 5 раз.
Токсикологи заявляют, что болгарин выпил не менее двух литров 40-градусного алкогольного напитка. Не смотря на это жизнь пациента вне опасности. Прежний рекорд был зафиксирован в 2003 году. Тогда в крови латыша нашли 7,22 промилле алкоголя.
А в феврале 2001 года в той же Латвии было обнаружено тело мужчины 30 лет, содержание алкоголя в крови у которого достигало 8,25 промилле. Впрочем, этому рекордсмену выжить не удалось.
Для справки: уровень содержания алкоголя в крови в 0,2 промилле соответствует одному стакану красного вина или двум бутылкам пива емкостью 0,33 литра, выпитым мужчиной средних лет и среднего веса на голодный желудок.
Калькулятор алкоголя онлайн: быстрый и точный
Наш калькулятор алкоголя в промилле рассчитывает концентрацию спирта в крови и ориентировочное время его выведения из организма. Сервис работает на основе всемирно признанной формулы Видмарка (Widmark Erik M. P.), дающей самые точные результаты.
Сервис работает на основе всемирно признанной формулы Видмарка (Widmark Erik M. P.), дающей самые точные результаты.
Идет подсчет…
Введите слева исходные данные
Максимальная концентрация
(Соответствует в выдыхаемом воздухе)
Указанная концентрация соответствует
Время выведения из организма
Инструкция. Чтобы воспользоваться алкогольным калькулятором, нужно ввести: пол, вес, рост человека, степень наполненности желудка, крепость и количество выпитого спиртного. Затем нажать на кнопку «Вычислить». Калькулятор рассчитает максимальную концентрацию этилового спирта, степень опьянения и время до полного выведения алкоголя из организма.
Состоянием на 2017 год, согласно ст.12.8 КоАП РФ, ответственность за вождение в нетрезвом виде: «наступает в случае установленного факта употребления вызывающих алкогольное опьянение веществ, который определяется наличием абсолютного этилового спирта в концентрации, превышающей возможную суммарную погрешность измерений, а именно 0,16 миллиграмма на один литр выдыхаемого воздуха». Это количество примерно соответствует 0,3 промилле (0,3 г алкоголя на 1 л крови).
Это количество примерно соответствует 0,3 промилле (0,3 г алкоголя на 1 л крови).
Внимание! Результаты вычислений не являются доказательством в суде и не служат основанием для оспаривания других способов (лабораторного или замера алкотестером). Время выведения алкоголя у каждого человека индивидуально, по формуле можно рассчитать лишь средние значения. Владелец сайта и разработчики калькулятора снимают с себя любую ответственность, связанную с его использованием.
Степени опьянения человека
Легкая (0,5-1,5 промилле) – наступает в первые минуты после употребления алкоголя. Мышцы расслабляются, улучшается настроение, появляется чувство комфорта. Человек становится общительным, смелым, излишне активным.
Средняя (1,5-2,5‰) – речь монотонная, иногда невнятная. Нарушается координация движений. Появляется раздражительность, грубость к окружающим или незнакомцам, агрессия. При средней степени опьянения большинство людей готовы затеять ссору или драку. Случаются кратковременные провалы памяти.
Случаются кратковременные провалы памяти.
Сильная (2,5-3,0‰) – координация полностью теряется, речь невнятная, часто сопровождающаяся полной потерей памяти. Зачастую при сильном опьянении человек теряет сознание, может наблюдаться непроизвольное мочеиспускание.
Алкогольное отравление (3-5‰) – чревато потерей здоровья или летальным исходом. Концентрация выше 5‰ считается смертельной дозой алкоголя, при которой спасти потерпевшего можно только в медицинском учреждении.
Если у вас возникли вопросы по работе нашего калькулятора выведения алкоголя из крови, вы можете задать их в комментариях.
Штрафы в Германии – ч. 2. Что грозит за управление транспортным средством после употребления алкоголя?
Вождение транспортного средства под воздействием алкоголя может быть в Германии определено как правонарушение или как преступление. Квалификация зависит от концентрации алкоголя в крови. Таким образом, когда водитель отвечает за нарушение, а когда за преступление и какое наказание ему угрожает?
В соответствии с § 316 Strafgesetzbuch (StGB – Уголовный кодекс) преступление совершает тот, кто в дорожном движении управляет транспортным средством, несмотря на то, что в результате употребления алкогольных напитков или других опьяняющих средств, не в состоянии безопасно вести.
Из всего вышесказанного можно сделать вывод, что водитель автомашины, имеющий содержание алкоголя в крови от 1,1 промилле, неспособен к вождению автомобиля. В таком случае говорится о полной неспособности к вождению.
При содержании алкоголя в крови в пределах 0,3-1,09 промилле, а также при установлении вызванной употреблением алкоголя неуверенности при управлении автомобилем – говорится о так называемой относительной неспособности к вождению, которая также может подвергаться наказанию согласно § 316 StGB. Примером этого являются: движение «зигзагом», особенно безрассудная или опасная езда.
В случае вождения под воздействием наркотических средств судебная практика не признает абсолютных границ действующих веществ. Из-за этого здесь нет речи о полной неспособности к вождению. Кроме того, следует принять решение в конкретном индивидуальном случае на основе употребленных и доказанных веществ и, в частности, на основе определенной концентрации активных веществ и ее последствий для безопасности вождения.
Вождение под воздействием алкоголя в уголовном процессе может быть доказано только на основании результата анализа крови. Судебная практика не признает результатов измерения концентрации алкоголя в выдыхаемом воздухе.
Когда правонарушение, а когда преступление?Правонарушение вождение под воздействием алкоголя может быть совершено умышленно (§ 316 абз. 1 StGB) или непреднамеренно (абз. 2). Из общепринятой судебной практики следует, что об умышленном вождении нельзя утверждать только на основании степени опьянения.
Юридическим последствием вождения под воздействием алкоголя, согласно § 316 StGB, является возможность наказания в виде лишения свободы до одного года или штрафом. Водитель механического транспортного средства, который до сих пор еще не был отмечен в полицейских базах и был впервые задержан, и у которого была обнаружена концентрация алкоголя в крови, превышающая 1,1 промилле, может получить штраф в размере от 30 до 50 ежедневных ставок (в зависимости от степени опьянения и степени его вины – т. е. умышленного или непреднамеренного действия).
е. умышленного или непреднамеренного действия).
Кроме того, водитель механического транспортного средства, управляющий в состоянии опьянения, регулярно лишается водительских прав – в соответствии с § 69 абз. 1, абз. 2 №2 StGB. Водитель, имея содержание алкоголя от 1,1 промилле, должен считаться с запретом на вождение транспортных средств на срок не менее девяти месяцев.
После истечения срока запрета водитель, лишенный водительских прав, должен обратиться в управление коммуникации с просьбой выдать новые водительские права, что в данном, конкретном случае может быть связано с многими трудностями (например, прохождением принудительных психологических исследований – с нем. Idiotentest).
Угроза для жизни и здоровья других людей наказывается строжеЕсли водитель, управляющий ТС под воздействием алкоголя или других наркотических средств, вследствие состояния алкогольного опьянения будет угрожать здоровью и жизни других лиц или чужим материальным ценностям, то из положения § 315c абз. 1, № 1а StGB следует, что это может привести к более высокими наказаниями (до трех лет лишения свободы, в случае умышленного нарушения – до пяти лет).
1, № 1а StGB следует, что это может привести к более высокими наказаниями (до трех лет лишения свободы, в случае умышленного нарушения – до пяти лет).
На практике приведение к опасности дорожного движения в соответствии с § 315c абз. 1 № 1а StGB (в результате употребления алкогольных напитков или других наркотических средств) частично приводит к определению явно более высоких штрафов, чем в случае, если упомянутое выше вождение под воздействием алкоголя без последствий, следующее из § 316 StGB.
В зависимости от того, закончилось ли это только на угрозе, или имел место ущерб, в этом случае зависит от суммы ущерба. Особенно, когда произошел ущерб здоровью других участников дорожного движения.
Если дело дойдет до случайного причинения смерти другому лицу водителем, находящимся под воздействием алкоголя или наркотических средств, виновный, который совершил преступления впервые, может получить наказание в виде лишения свободы, исполнение которого не приостанавливается на испытательный срок.
Юридические уголовные санкции вступают в силу в соответствии с § 315c абз. 1, № 2, абз. 3 StGB также в случае особенно тяжелых проступков водителей механических транспортных средств, не допущенных под воздействием алкоголя или наркотических средств, но серьезным образом не соответствующих требованиям правил дорожного движения и абсолютных, которые ведут к угрозе жизни и здоровью другого человека или чужого имущества большой ценности.
Правонарушение – нарушение так называемой границы 0,5 промилле содержания алкоголя в кровиВ соответствии с § 24, абз. 1, StVG, правонарушение совершает тот, кто ведет транспортное средство в дорожном движении, имея в выдыхаемом воздухе содержание алкоголя 0,25 мг или больше или содержание алкоголя в крови 0,5 промилле или больше.
Иначе, чем в рамках преступлений, можно сделать вывод уже из положений закона, что в рамках доказательства достаточным является результат анализа выдыхаемого воздуха. Значение 0,25 мг/л алкоголя в выдыхаемом воздухе согласно научным данным соответствует примерно 0,5 промилле алкоголя в крови.
В соответствии с § 24 абз. 2 StVG совершает правонарушение тот, кто под воздействием наркотических средств ведет механическое транспортное средство. Закон указывает здесь на приложение к положению § 24 StVG, указывающему все распространенные наркотические средства. Закон определяет в положении § 24, абз. 2, предложение 2, что такой эффект имеет место, если в крови доказано существование веществ, перечисленных в вышеуказанном приложении (например, THC или MDMA).
Однако для такого утверждения недостаточным является любое количество активных веществ, которые можно доказать даже с использованием самых современных технических средств. Концентрация активных веществ, которая позволяет предположить, что способность водителя к вождению механических транспортных средств была ограничена, должна быть четко более нуля. Начиная с концентрации 1 нг/мл THC судебная практика принимает действие в описанном выше понимании и, следовательно, ввиду совершения правонарушения согласно § 24а, абз. 2 StVG.
2 StVG.
Правонарушение, согласно § 24а, абз. 4 StGB может быть наказано штрафом до 3 тыс. евро. Согласно используемому здесь каталогу штрафов, преступник, который совершил преступление впервые, должен считаться со штрафом в размере 500 евро, а рецидивист – со штрафом в размере 1 тыс. евро. В соответствии с § 25 StGB кроме того, можно наложить на данного водителя запрет на вождение от одного до трех месяцев. Преступник, который совершил преступление впервые, должен считаться с запретом на вождение автомобиля на один месяц, рецидивист – на два-три месяца.
Запрет на вождение транспортных средств означает только то, что человек не должен в течение установленного срока управлять автотранспортными средствами в дорожном движении. На это время он должен отдать свои водительские права в официальный депозит. После истечения запрета он может беспрепятственно использовать свои водительские права.
В этом отношении запрет на вождение механических транспортных средств является средством явно более мягким, чем лишение водительских прав. Интересно, что в случае, если концентрация алкоголя в крови составляет от 0,30 до 0,49 промилле, мы не имеем дела даже с нарушением, но если до этого дойдут вызванные алкоголем ошибки водителя, можно говорить о наличии преступления по § 315c абз.
Интересно, что в случае, если концентрация алкоголя в крови составляет от 0,30 до 0,49 промилле, мы не имеем дела даже с нарушением, но если до этого дойдут вызванные алкоголем ошибки водителя, можно говорить о наличии преступления по § 315c абз.
| Поступок | Штраф в евро | Штрафные пункты | Запрет на вождение автомобиля |
| Незначительное превышение 0,5 промилле | – | – | – |
| 1 нарушение | 500 | 2 | 1 месяц |
| 2 нарушение | 1000 | 2 | 1 месяц |
| 3 нарушение | 1500 | 2 | 1 месяц |
| Опасность для дорожного движения (от 0,3 промилле) | – | 3 | 1 месяц |
| Значение алкоголя в крови выше 1,09 промилле | – | 3 | 1 месяц |
Когда-то в Германии у моего клиента задержали водительские права за вождение после употребления алкоголя. Затем, когда я получал документ из полиции, мне пришлось предоставить справку о том, что задержанный не алкоголик. Врач выдает ее на основании исследования функции печени.
Затем, когда я получал документ из полиции, мне пришлось предоставить справку о том, что задержанный не алкоголик. Врач выдает ее на основании исследования функции печени.
Езда в нетрезвом виде: юрист составил памятку для автомобилистов | Эстония
Присяжный адвокат Дмитрий Школяр составил для читателе порталов ERR.ee короткий обзор на основании своего многолетнего опыта.
«Из-за большого объема невозможно охватить абсолютно все вопросы, связанные с данной темой, поэтому постараюсь ответить именно на те вопросы, которые люди чаще всего задают, и к которым проявляют особый интерес», — сказал Школяр.
1. Что такое состояние опьянения?
Если коротко, то состояние опьянения — это нахождение в состоянии алкогольного или наркотического опьянения.
В соответствии с частью 1 статьи 36 Закона об охране общественного порядка, состояние опьянения — это обусловленное употреблением алкоголя, наркотических средств или психотропных веществ, или иных опьяняющих веществ состояние здоровья, которое проявляется в нарушении либо изменении физических или психических функций и реакций.
1.2. Алкогольное опьянение: промилле и миллиграммы
В промилле измеряется содержание алкоголя в крови.
Другой распространенной единицей измерения является миллиграмм на литр (мг/л) выдыхаемого воздуха. Если измерение содержание алкоголя происходит с помощью выдыхаемого воздуха, то измеряется содержание этанола в одном литре выдыхаемого воздуха. При этом, для расчета содержащегося в крови количества алкоголя применяется общепризнанное соотношение 1:2100. Другими словами, 1 миллиграмм этанола в одном литре (1 мг/л) выдыхаемого воздуха считается равным 2,1 промилле алкоголя.
В суде в качестве доказательства принимаются только показатели калибрированного доказательственного алкометра, показывающие содержание алкоголя в мг/л. Также имеют в суде силу доказательства и результаты анализов крови.
Хотя широко распространенные в полиции индикативные приборы (так называемые “трубки”) для установления опьянения показывают результаты измерения в конкретных цифрах, их используют в основном для того, чтобы определить имеется ли дело с алкогольным опьянением. Если индикативным прибором установлено алкогольное опьянение, то после этого полиция уже использует калибрированный доказательственный прибор, показывающий содержание алкоголя в мг/л. По этой причине и дается, как правило, возможность подуть в два разных алкометра, сначала в индикативый прибор, а затем уже в доказательственный, если показания индикативного прибора указывают на наличие алкогольного опьянения. Использование индикативного прибора не является обязательным, если имеется доказательственный алкометр.
Если индикативным прибором установлено алкогольное опьянение, то после этого полиция уже использует калибрированный доказательственный прибор, показывающий содержание алкоголя в мг/л. По этой причине и дается, как правило, возможность подуть в два разных алкометра, сначала в индикативый прибор, а затем уже в доказательственный, если показания индикативного прибора указывают на наличие алкогольного опьянения. Использование индикативного прибора не является обязательным, если имеется доказательственный алкометр.
1.3. Наркотическое опьянение
Наркотическое опьянение проверяется с помощью быстрых тестов. Водитель с подозрением на наркотическое опьянение доставляется на экспертизу в медицинское учреждение, где наличие наркотических или психотропных веществ, или иных опьяняющих веществ устанавливается путем исследования биологической жидкости (кровь, моча).
Так как не существует прибора, похожего на алкометр, который мог бы за считанные секунды установить наркоопьянение, то расследование по делам с наркоопьянением занимает немного больше времени.
2. В чем состоит управление в нетрезвом виде?
Наказуемое управление механическим транспортным средством состоит из двух признаков:
— водитель находится в состоянии опьянения,
— управляет механическим транспортным средством (автомобиль, мотоцикл, мопед), вездеходом (АTV и тд), трамваем, находясь в состоянии опьянения.
К управлению механическим транспортным средством приравниваются действия лица, которые оно совершает не на месте водителя, но которыми оно при помощи устройств управления (руль управления, рулевое колесо и т. п.) оказывает воздействие на направление или скорость движения механического транспортного средства. Обращаю внимание, что управление транспортным средством начинается сразу, как только водитель начинает движение.
Запрет на управление транспортным средством действует везде, как на дорогах, так и вне дорог, например, на безлюдном поле, находящемся вдалеке от населенных пунктов.
3. Какое количество алкоголя считается допустимым?
Можно сказать, что в Эстонии действует нулевая терпимость в отношении вождения в нетрезвом виде. Считается, что от 0,01 до 0,19 промилле является физиологическим содержанием алкоголя в организме либо связанное с питанием увеличение содержания алкоголя. Такое содержание алкоголя в организме не наказуемо.
Считается, что от 0,01 до 0,19 промилле является физиологическим содержанием алкоголя в организме либо связанное с питанием увеличение содержания алкоголя. Такое содержание алкоголя в организме не наказуемо.
Таким образом, содержания алкоголя в выдыхаемом воздухе не должно превышать 0,2 промилле (то есть 0,10 мг/л).
4. Границы алкогольного опьянения и виды ответственности
4.1. Проступок
Если у водителя содержание алкоголя составляет от 0,10 до 0,74 мг/л в выдыхаемом воздухе (от 0,2 до 1,49 промилле), то такое деяние является проступком.
4.2. Преступление
Содержание алкоголя 0,75 мг/л в выдыхаемом воздухе (1,5 промилле) и выше является преступлением, за которое предусмотрена уголовная ответственность.
Если водитель находится в опьянении, возникшим от употребления наркотического средства или психотропного вещества, то полиция также начинает уголовное производство.
5.Что может потребовать водитель, если он не считает себя пьяным?
Водитель имеет право отказаться дуть в индикативный алкометр или отказаться от проверки опьянения доказательственным алкометром и потребовать проверить содержание алкоголя в крови. Полиция должна информировать водителя о том, что у него есть такое право, о чем полицейский делает отметку в протоколе и берет подпись водителя. В таком случае, полиция, по требованию водителя доставляет его в медицинское или государственное экспертное учреждение, чтобы взять анализ крови и определить содержание алкоголя с помощью экспертизы.
Полиция должна информировать водителя о том, что у него есть такое право, о чем полицейский делает отметку в протоколе и берет подпись водителя. В таком случае, полиция, по требованию водителя доставляет его в медицинское или государственное экспертное учреждение, чтобы взять анализ крови и определить содержание алкоголя с помощью экспертизы.
Кроме того, полиция может доставить водителя на экспертизу по своему усмотрению, если водитель находится в таком состоянии, что неспособен подуть в алкометр.
В отдельных случаях полиция может использовать принуждение для взятия пробы крови.
6. Вкратце о производстве по проступку
Как уже говорилось, если водитель употребил алкоголь выше допустимого предела, предусмотренного Законом о дорожном движении, то есть, в диапазоне от 0,20 до 1,49 промилле, то водителя привлекают к ответственности в порядке проступка. Полиция начинает дело о проступке, выносит решение об отстранении водителя от управления автомобилем, в общем производстве составляет протокол о проступке (в ускоренном производстве протокол о проступке не составляется). Также у полиции есть право доставить водителя на вытрезвление или задержать его на срок до 48 часов.
Также у полиции есть право доставить водителя на вытрезвление или задержать его на срок до 48 часов.
В протоколе о проступке указывается, начиная с какого дня будет доступно для ознакомления решение полиции по делу о проступке.
Полиция выносит решение по делу как правило в течение 1 месяца со дня составления протокола о проступке.
Если водитель не согласен с решением полиции, то он может подать на решение жалобу в уездный суд. Жалоба подается в течение 15 дней, начиная со дня, когда решение полиции стало доступным для ознакомления.
Обращаю внимание, что полиция не обязана сама вручать водителю решение по делу о проступке. Это значит, что решение полиции никто не будет высылать вам домой. Необходимо самому прийти в полицию за решением либо получить его в электронном виде с помощью e-toimik. Решение полиции вступает в силу по истечении 15 дней, считая со дня, когда решение стало доступно для ознакомления независимо от того, явилось лицо за ним или нет.
Вступившее в силу решение полиции обжаловать нельзя.
7. Наказания в порядке проступка за вождение в состоянии опьянения (§ 224 Закона о дорожном движении)
7.1. Если в одном литре выдыхаемого воздуха содержание алкоголя 0,10-0,24 миллиграмма, то такое деяние наказывается штрафом до 100 штрафных единиц или лишением права управления на срок до 6 месяцев.
7.2. Если в одном литре выдыхаемого воздуха содержание алкоголя 0,25-0,74 миллиграмма, то такое деяние наказывается штрафом до 300 штрафных единиц или лишением права управления на срок до 12 месяцев.
8. Как понимается назначенное за проступок наказание?
Наказание за управление механическим транспортным средством в порядке проступка может состоять из двух частей:
— основное наказание (штраф или арест, или лишение прав),
— дополнительное наказание (лишение прав).
8.1. Основное наказание за проступок:
Штраф. Суд или полиция (лицо, ведущее внесудебное производство) могут наложить штраф в размере от 3 до 300 штрафных единиц. Штрафной единицей является базовая сумма штрафа, размер которой составляет 4 евро (по состоянию на 2015 год). Таким образом, максимальный размер штрафа за проступок составляет 1200 евро, минимальный — 12 евро.
Штрафной единицей является базовая сумма штрафа, размер которой составляет 4 евро (по состоянию на 2015 год). Таким образом, максимальный размер штрафа за проступок составляет 1200 евро, минимальный — 12 евро.
Арест. Суд может назначить за проступок арест сроком до 30 суток. Арест может быть назначен только судом. В случае, если полиция считает необходимым ходатайствовать о назначении водителю ареста, лицо вызывается на судебное заседание для рассмотрения дела о проступке.
Лишение права управления. Суд или полиция может назначить за проступок в качестве основного наказания лишение права управления транспортным средством на срок до 2 лет.
Штраф и арест не могут быть назначены одновременно, так как применяться может только одно из основных наказаний.
8.2. Дополнительное наказание за проступок: лишение права управления на срок от 3 до 12 месяцев
Как видно, закон предусматривает возможность применения лишения права управления как в качестве основного, так и дополнительного наказания. Однако, законом запрещено применение лишения права управления одновременно как основного и дополнительного наказания. Это означает, что если полиция или суд считают необходимым лишить водителя прав, то при назначении наказания необходимо взвесить, будет ли применено только лишение прав (основное наказание) или применить, например, штраф и лишение прав (основное + дополнительное наказание). Разница заключается в сроке, на который лишают прав управления: лишение прав как дополнительное наказание ограничено 12 месяцами.
Однако, законом запрещено применение лишения права управления одновременно как основного и дополнительного наказания. Это означает, что если полиция или суд считают необходимым лишить водителя прав, то при назначении наказания необходимо взвесить, будет ли применено только лишение прав (основное наказание) или применить, например, штраф и лишение прав (основное + дополнительное наказание). Разница заключается в сроке, на который лишают прав управления: лишение прав как дополнительное наказание ограничено 12 месяцами.
8.3. Иная мера воздействия на водителя за проступок
Вынося наказание за вождение в нетрезвом виде, суд может применить наряду с наказанием еще и меры воздействия на водителя. Суд может конфисковать транспортное средство как средство совершения виновного деяния. Как правило, конфискация транспортного средства применяется в судебной практике в случаях, когда водителя уже наказывали за аналогичные правонарушения и наказания являются действующими (то есть, наказание не исполнено, либо правонарушения совершены в течение короткого времени).
9. В каких случаях начинают уголовное производство за вождение в состоянии опьянения?
Выше уже отмечалось, что если водитель находится в состоянии наркотического опьянения или алкогольное опьянение составляет по крайней мере 0,75 мг/л (1,5 промилле), полиция начинает уголовное производство по делу. Установив у водителя алкогольное опьянение, полиция выносит решение об отстранении водителя от управления автомобилем и, как правило, водителя сразу задерживают в качестве подозреваемого по уголовному делу. Задержание в качестве подозреваемого означает лишение свободы на срок до 48 часов. Полиция доставляет задержанного в отдел полиции или в арестный дом. После того, как следователь проведет с задержанным необходимые процессуальные действия, задержанного либо освобождают, либо полиция доставляет задержанного в суд для рассмотрения уголовного дела.
10. Вкратце о рассмотрении уголовного дела в уездном суде
Если обстоятельства совершения преступления ясны, и в течение короткого времени собраны все необходимые доказательства, то прокуратура может ходатайствовать перед судом о рассмотрении дела в ускоренном производстве. В основном, уголовные дела, связанные с вождением в нетрезвом виде, рассматриваются в судах именно в ускоренном производстве.
В основном, уголовные дела, связанные с вождением в нетрезвом виде, рассматриваются в судах именно в ускоренном производстве.
Ускоренное производство означает, что разбирательство по делу в полиции и в суде возможно провести в течение 48 часов с момента задержания нетрезвого водителя и до вынесения решения в суде. Практика показывает, что, как правило, задержанного водителя домой не отпускают, полиция проводит с ним следственные действия и сразу передает материалы дела в прокуратуру, а прокурор уже передает материалы в суд. Полиция доставляет задержанного водителя в суд, где прокурор предъявляет обвинение и проходит судебное разбирательство. После заседания судья выносит решение по уголовному делу. Суд может вынести оправдательный или обвинительный приговор. Если суд признает обвиняемого виновным, то назначается уголовное наказание. Если суд оправдал обвиняемого или же вынес наказание, которое не связано с реальным тюремным заключением, то обвиняемый освобождается в зале суда. На практике вся эта процедура в ускоренном производстве занимает 2-3 дня (до 48 часов). Участие адвоката в ускоренном производстве обязательно.
Участие адвоката в ускоренном производстве обязательно.
Если по каким-то причинам невозможно применить ускоренное производство, то уголовное дело продолжается в другом виде производства, в таком случае задержанного либо освобождают, либо берут под стражу, если суд даст на это разрешение.
11. Уголовное наказание за вождение в состоянии опьянения (Пенитенциарный кодекс § 424)
Уголовное наказание за управление механическим транспортным средством может состоять из двух частей (как и в случае с проступком): основное и дополнительное наказание.
11.1. Основное наказание за преступление: (ПК § 424) — денежное наказание или тюремное заключение. Вид и размер наказания избирает суд, учитывая, прежде всего, размер вины обвиняемого, а также прочие данные, влияющие на решение суда.
Денежное наказание. Вынося обвинительный приговор, суд может наказать за вождение в нетрезвом виде денежным наказанием в размере от 30 до 500 дневных ставок. Минимальный размер одной дневной ставки составляет 10 евро (по состоянию на 2015 год). При назначении денежного наказания за основу берется минимальная ставка в 10 евро, однако если дневной доход обвиняемого превышает 10 евро, то за основу берется дневной доход обвиняемого, а не минимум. Например, если ежедневный доход обвиняемого составляет 40 евро, то размер денежного наказания рассчитывается на основании 40 евро, а не 10. Данные о среднем дневном доходе берутся из базы данных Налогово-таможенного департамента. Если обвиняемый является безработным, то применение денежного наказания маловероятно, так как у обвиняемого нет реальной возможности оплатить, то есть, исполнить наказание. Доход супруга или родственников не играют решающую роль в этом случае, поскольку наказания применяются все-таки к конкретному обвиняемому, а не к членам его семьи.
Минимальный размер одной дневной ставки составляет 10 евро (по состоянию на 2015 год). При назначении денежного наказания за основу берется минимальная ставка в 10 евро, однако если дневной доход обвиняемого превышает 10 евро, то за основу берется дневной доход обвиняемого, а не минимум. Например, если ежедневный доход обвиняемого составляет 40 евро, то размер денежного наказания рассчитывается на основании 40 евро, а не 10. Данные о среднем дневном доходе берутся из базы данных Налогово-таможенного департамента. Если обвиняемый является безработным, то применение денежного наказания маловероятно, так как у обвиняемого нет реальной возможности оплатить, то есть, исполнить наказание. Доход супруга или родственников не играют решающую роль в этом случае, поскольку наказания применяются все-таки к конкретному обвиняемому, а не к членам его семьи.
Тюремное заключение. За вождение в состоянии опьянения суд может назначить тюремное заключение на срок от 1 месяца до 3 лет. Тюремное заключение может быть назначено реально или условно. Если суд назначил условное тюремное заключение, то осужденный не должен сидеть в тюрьме, однако ему будет назначен испытательный срок, в течение которого за поведением осужденного может быть особый контроль.
Тюремное заключение может быть назначено реально или условно. Если суд назначил условное тюремное заключение, то осужденный не должен сидеть в тюрьме, однако ему будет назначен испытательный срок, в течение которого за поведением осужденного может быть особый контроль.
11.2. Дополнительное наказание за преступление (ПК § 50)
В качестве дополнительного наказания суд может лишить водителя права управления механическим транспортным средством на срок от 1 месяца до 3 лет. Если суд применяет дополнительное наказание и лишает водительских прав, то осужденный обязан в течение 5 рабочих дней со дня вступления в силу приговора суда сдать права в Департамент шоссейных дорог (Maanteeamet). В судебной практике применение одновременно основного и дополнительного наказания получило широкое распространение уже давно.
Права на управление механическим транспортным средством нельзя лишить человека, который использует автомашину в связи с нарушением двигательных функций организма.
11.3. Иная мера воздействия на водителя за преступление
Вынося наказание за вождение в нетрезвом виде, суд может конфисковать транспортное средство как средство совершения преступления. Как уже говорилось выше, конфискация транспортного средства применяется в судебной практике в случаях, когда водителя уже наказывали за аналогичные правонарушения и наказания являются действующими (то есть, наказание не исполнено, либо правонарушения совершены в течение короткого времени)
12. Подробнее о водительских правах
12.1. Если суд лишил водительских прав, то права необходимо отнести в Департамент шоссейных дорог. Обращаю внимание еще раз на то, что если вступило в силу решение о приостановлении, лишении или признании недействительным действия водительских прав, то лицо обязано в течение пяти рабочих дней со дня вступления в силу такого решения сдать права в Департамент шоссейных дорог. Если лицо не соблюдает это требование, то Департамент шоссейных дорог может наложить штраф в размере до 640 EUR. Тут следует отметить, что наличие водительских прав на руках у водителя еще не означает, что права действительны.
Тут следует отметить, что наличие водительских прав на руках у водителя еще не означает, что права действительны.
12.2. Восстановление водительских прав
Если водителя в качестве наказания лишили права управлять механическим транспортным на срок от 6 до 12 месяцев, то права можно восстановить при условии, что лицо успешно сдаст экзамен по теории. Если наказанием предусмотрено лишение прав на срок 12 месяцев или дольше, то права могут восстановлены, если лицо успешно сдаст экзамен, состоящий из двух частей: теория и вождение.
Если срок лишения прав составляет менее 6 месяцев, то сдавать экзамены не следует, действие прав будет восстановлено, когда закончится действие наказания. Никогда не рассчитывайте самостоятельно дату восстановления действия прав! Проконсультируйтесь с чиновником Департамента шоссейных дорог, в противном случае может случиться, что вы сядете за руль в то время, когда еще не восстановлено право управления. В таком случае, водителя ожидает новое уголовное дело.
12.3. Езда без прав во время действия дополнительного наказания
Ни в коем случае нельзя управлять транспортным средством в период, когда действует лишение прав. Если лишение прав было назначено судом, то езда без прав (даже в трезвом виде) будет квалифицироваться как уклонение от исполнения наказания (§ 329 ПК) и полиция начнет новое уголовное дело в отношении водителя. Процедура по уголовному делу будет, скорее всего, такая же как за вождение в нетрезвом виде, что было описано выше.
Кроме того, стоит особо обратить внимание на то, что с 01.01.2015 вступила в силу новая статья Пенитенциарного кодекса, предусматривающая уголовную ответственность за систематическую (3 раза) езду без прав (§ 4231 ПК). До появления этой статьи в кодексе систематически вождение без прав являлось не преступлением, а проступком.
13. Что еще следует знать каждому собственнику (или владельцу) автомобиля о вождении в нетрезвом виде?
Лицо можно привлечь к ответственности, даже если он сам не управлял автомобилем в состоянии алкогольного опьянения.
Я имею в виду ситуации, когда владелец машины, например, не садится за руль сам, но позволяет управлять машиной своему нетрезвому другу. § 225 Закона о дорожном движении предусматривает, что допуск собственником, владельцем или водителем механического транспортного средства, вездехода или трамвая к управлению механическим транспортным средством, вездеходом или трамваем лица, находящегося в состоянии опьянения или передача ему управления наказывается штрафом в размере до трехсот штрафных единиц (то есть, до 1200 евро). В таком случае, к ответственности будут привлечены оба лица — нетрезвый водитель и владелец автомобиля.
14. В заключение: планы Департамента полиции в 2015 году
Минимальное количество водителей, подлежащих плановому контролю на наличие опьянения:
Пыхьяская префектура 218 327 человек
Лыунаская префектура 250 750 человек
Идаская префектура 123 159 человек
Ляянеская префектура 107 764 человек
Участники ДТП также подлежат проверке на предмет употребления алкогольных, наркотических или психотропных веществ.
В крови погибшего ребенка опять нашли алкоголь. Его сбил полицейский
Автор фото, Artyom Geodakyan/TASS
Подпись к фото,Архивное фото
В Кировской области родители шестилетнего мальчика, которого на автомобиле задавил полицейский, получили результаты экспертизы, согласно которой в крови ребенка был алкоголь. Это второй такой случай, он вызвал резонанс, и глава СКР потребовал провести новую экспертизу.
Как пишет ТАСС со ссылкой на кировское издание Newsler.ru, родители погибшего мальчика получили результаты судмедэкспертизы на днях. Она показала наличие в крови погибшего 0,51 промилле этанола.
Отсутствие влияния алкоголя наблюдается до значения 0,5 промилле, то есть оно в любом случае превышено, объясняет издание.
Ребенок погиб под колесами автомобиля 13 июля этого в селе Буйское Уржумского района Кировской области. Шестилетний мальчик ехал на велосипеде по грунтовой дороге в сторону асфальтовой трассы, по которой двигалась машина. За рулем оказался полицейский — оперативный дежурный дежурной части пункта полиции. По официальной информации, он был трезв.
За рулем оказался полицейский — оперативный дежурный дежурной части пункта полиции. По официальной информации, он был трезв.
Следственное управление по Кировской области расследует уголовное дело по ч. 3 ст. 264 УК РФ (нарушение правил дорожного движения). «Водитель продолжает работу в органах», — рассказала Newsler.ru знакомая семьи Татьяна Опарина.
В следственном управлении изданию подтвердили, что водитель, который сбил мальчика, «вылетевшего на дорогу на велосипеде», до сих пор работает в полиции, но заверили, что никакого негативного влияния на расследование он не оказывает.
«Родители хотят справедливости, чтобы виновные были наказаны. Но уголовное дело кидают из рук в руки разным следователям», — пожаловалась Опарина. «Про этанол следователь сказал, что, может быть, это природное содержание, то есть от каких-либо продуктов», — сообщила она.
Публикация кировского издания вызвала резонанс. О возмущении родственников узнали в Москве, и вечером во вторник Следственный комитет России (СКР) сообщил, что глава ведомства Александр Бастрыкин распорядился назначить повторные судебно-медицинские экспертизы.
В СМИ «появилась информация о том, что в крови у мальчика было обнаружено 0,51 промилле алкоголя», результаты экспертизы вызвали недоверие у родственников погибшего ребенка, которые «требуют объективного и всестороннего расследования», заявила представитель СКР Светлана Петренко.
Это уже второй такой случай, получивший большую огласку в прессе.
В 2017 году в подмосковной Балашихе местная жительница Ольга Алисова насмерть сбила шестилетнего мальчика. Было возбуждено уголовное дело, ей предъявили обвинение в нарушении правил дорожного движения, повлекшем смерть.
Судмедэксперты, проводившие исследование тела мальчика, вынесли заключение, согласно которому в его крови содержалось 2,7 промилле алкоголя, что соответствует высокой степени опьянения.
Повторная судебная экспертиза показала, что в крови погибшего ребенка алкоголя не было. Эксперт, ошибочно определивший алкоголь в крови ребенка, получил 10 месяцев исправительных работ.
Алкоголь попал в кровь шестилетнего ребенка, сбитого автомобилем во дворе жилого дома в Подмосковье, в результате неправильных действий судмедэксперта, не сумевшего предотвратить процесс брожения во взятой на анализ крови, сообщал тогда СКР.
Алисова была признана виновной и получила три года колонии-поселения. Бастрыкин в 2017 году также требовал передать в СКР дело о ДТП с «пьяным» мальчиком (так его называли в СМИ).
Калькулятор алкоголя онлайн: точный расчет в промиле
Наш онлайн калькулятор алкоголя в промилле (‰) поможет вам рассчитать концентрацию спирта в крови и в выдыхаемом воздухе с учетом времени приема алкоголя. В основе сервиса лежит признанная во всем мире формула шведского химика Эрика Матео Прохета Видмарка (Widmark Erik M. P.), которая считается наиболее точной и достоверной. Она дополнена с учетом среднестатистической скорости выведения алкоголя, а также некоторых физиологических особенностей организма.
Инструкция: Просто заполните все поля в калькуляторе.
Промилле – одна тысячная доля или 1/10 процента. В данном случае подразумевается количество этанола, содержащегося в 1 л крови (в смеси с чистым этанолом). Проще говоря, 1,5 ‰ концентрации значит, что в 1000 мл крови содержится 1, 5 мл чистого этанола. При этом учитывается именно объем, а не масса, поэтому разные по плотности напитки, но одинаковые по массе приведут к разным промилле.
Наш калькулятор показывает максимальную концентрацию чистого этанола в крови после единовременного употребления указанного вами объема алкоголя. Просим вас обратить внимание на то, что в расчетах не учитываются различные заболевания, состояние вашего организма и прочие физиологические составляющие, которые могут сильно повлиять на результат.
Также следует учитывать, что наш калькулятор использует средние значения таких показателей как дефицит резорбции (необъяснимая потеря алкоголя во время всасывания его в кровь; с пустым желудком потери составляют приблизительно 10%, с полным – приблизительно 30%), снижение концентрации алкоголя в крови за определенный промежуток времени (взято среднее значение в 0,15 ‰/ч) и т. д.
д.
Внимание! Вычисления вы проводите на собственный страх и риск. Результаты вычислений не могут использоваться вами как доказательства в суде, основания для судебных и прочих исков, равно как и для оспаривания результатов лабораторных исследований. Редакция сайта therumdiary.ru не несет ответственности за результаты расчетов и их последствия. Не пейте за рулем!
Степени опьянения
В первую очередь калькулятор будет полезен водителям. На основании полученных данных можно рассчитать время, через которое можно садиться за руль без риска и нежелательных последствий после употребления спиртных напитков. Это позволит вас уверенней чувствовать себя на дороге и избежать неуместных споров с сотрудниками ГИБДД.
Наш калькулятор способен с большой вероятностью определить, сколько чистого спирта поступило или же только поступит в кровь после возлияний. Это очень важная и актуальная информация, ведь за вождение в нетрезвом виде предусмотрены серьезные санкции (штрафы и лишение водительских прав на длительный срок). Также калькулятор полезен тем, кто хочет узнать дозу алкоголя, которая вызовет ту или иную степень опьянения, что может очень пригодится в период празднеств.
Также калькулятор полезен тем, кто хочет узнать дозу алкоголя, которая вызовет ту или иную степень опьянения, что может очень пригодится в период празднеств.
- до 0,5‰ – отсутствие влияния алкоголя;
- 0,6 – 1,5‰ – легкая степень опьянения, характеризуется притуплением ощущений, расторможенностью, экстравертностью, нарушением глубины восприятия, рассуждения, периферического зрения, приспосабливаемости зрачков.
- 1,5 – 2,0‰ – средняя степень опьянения, характеризуется сверх-экспрессиновтью, гневом или печалью, нарушением рефлексов, времени реакции, основных моторных навыков, членораздельной речи; малая вероятность алкогольного отравления.
- 2,0 – 3,0‰ – сильная степень опьянения, характеризуется ступором, потерей способности к пониманию, тяжелым нарушением моторики, потерей памяти, потерей сознания.
- 3,0 – 5,0‰ – тяжёлое отравление вплоть, характеризуется сильным угнетением ЦНС, потерей сознания, нарушением сердцебиения, дыхания, чувства равновесия; высокий риск отравления и смерти.

- более 5,0‰ – в большинстве случаев летальный исход.
Напомним, что государство в последние годы существенно ужесточило требования по допустимому уровню алкоголя (чистого спирта, т.е. этанола) в выдыхаемом воздухе и крови. Так, вас признают пьяным, если: концентрация чистого этанола в выдыхаемом воздухе превышает 0,16 мг/л, в крови – 0,35 промилле.
Вопросы относительно алкогольного калькулятора вы можете задать в комментариях на этой странице!
Оценить: Загрузка…Другие единицы для концентраций растворов
Результаты обучения
- Определите единицы концентрации: массовый процент, объемный процент, массово-объемный процент, доли на миллион (ppm) и доли на миллиард (ppb)
- Выполнение вычислений, связанных с концентрацией раствора и объемами и / или массами его компонентов
В предыдущем разделе мы ввели молярность, очень полезную единицу измерения для оценки концентрации растворов.Однако молярность — это только одна мера концентрации. В этом разделе мы познакомимся с некоторыми другими единицами концентрации, которые обычно используются в различных приложениях, либо для удобства, либо по соглашению.
В этом разделе мы познакомимся с некоторыми другими единицами концентрации, которые обычно используются в различных приложениях, либо для удобства, либо по соглашению.
Массовый процент
Ранее мы узнали о процентном составе как мере относительного количества данного элемента в соединении. Проценты также обычно используются для выражения состава смесей, включая растворы. Массовый процент компонента раствора определяется как отношение массы компонента к массе раствора, выраженное в процентах:
[латекс] \ text {массовый процент} = \ dfrac {\ text {масса компонента}} {\ text {масса раствора}} \ times 100 \% [/ latex]
Обычно нас больше всего интересует массовый процент растворенных веществ, но также возможно вычислить массовый процент растворителя.
Массовый процент также упоминается схожими названиями, такими как массовых процента, массовых процентов, массовых процентов и других вариаций на эту тему. Наиболее распространенный символ массового процента — это просто знак процента,%, хотя часто используются более подробные символы, включая% массы,% веса и (вес / вес)%. Использование этих более подробных символов может предотвратить смешение массовых процентов с другими типами процентов, такими как объемные проценты (которые будут обсуждаться позже в этом разделе).
Использование этих более подробных символов может предотвратить смешение массовых процентов с другими типами процентов, такими как объемные проценты (которые будут обсуждаться позже в этом разделе).
Массовые проценты — популярные единицы концентрации для потребительских товаров. На этикетке типичного флакона с жидким отбеливателем (рис. 1) указано, что концентрация его активного ингредиента, гипохлорита натрия (NaOCl), составляет 7,4%. Таким образом, образец отбеливателя весом 100,0 г будет содержать 7,4 г NaOCl.
Рис. 1. Жидкий отбеливатель представляет собой водный раствор гипохлорита натрия (NaOCl). Эта марка имеет концентрацию NaOCl 7,4% по массе.
Пример 1:
Расчет массового процентаА 5.Образец спинномозговой жидкости 0 г содержит 3,75 мг (0,00375 г) глюкозы. Каков процент глюкозы в спинномозговой жидкости по массе?
Показать решение Образец спинномозговой жидкости содержит примерно 4 мг глюкозы в 5000 мг жидкости, поэтому массовая доля глюкозы должна быть немного меньше одной части на 1000, или около 0,1%. Подставляя данные массы в уравнение, определяющее массовые проценты, получаем:
Подставляя данные массы в уравнение, определяющее массовые проценты, получаем:
[латекс] \% \ text {глюкоза} = \ dfrac {3,75 \ text {мг глюкозы} \ times \ frac {1 \ text {g}} {1000 \ text {мг}}} {5.0 \ text {g спинномозговой жидкости}} = 0,075 \% [/ latex]
Рассчитанный массовый процент соответствует нашей приблизительной оценке (немного меньше 0,1%).
Обратите внимание, что хотя любая единица массы может использоваться для вычисления массового процента (мг, г, кг, унция и т. Д.), Одна и та же единица должна использоваться как для растворенного вещества, так и для раствора, так что единицы массы сокращаются, давая безразмерное соотношение. В этом случае мы преобразовали единицы растворенного вещества в числителе из мг в г, чтобы они соответствовали единицам в знаменателе. С таким же успехом мы могли бы вместо этого преобразовать знаменатель с г в мг.Если для растворенного вещества и раствора используются одинаковые единицы массы, вычисленный массовый процент будет правильным.
Флакон средства для чистки плитки содержит 135 г HCl и 775 г воды. Какой процент по массе HCl в этом очищающем средстве?
Пример 2:
Расчеты с использованием массового процента«Концентрированная» соляная кислота — это водный раствор 37,2% HCl, который обычно используется в качестве лабораторного реагента.Плотность этого раствора 1,19 г / мл. Какая масса HCl содержится в 0,500 л этого раствора?
Показать решение Концентрация HCl составляет около 40%, поэтому порция этого раствора в 100 г будет содержать около 40 г HCl. Поскольку плотность раствора не сильно отличается от плотности воды (1 г / мл), разумная оценка массы HCl в 500 г (0,5 л) раствора примерно в пять раз больше, чем в 100 г порции, или [латекс] 5 \ times 40 = 200 \ text {g.} [/ latex] Чтобы вывести массу растворенного вещества в растворе из его массового процента, нам нужно знать соответствующую массу раствора. Используя заданную плотность раствора, мы можем преобразовать объем раствора в массу, а затем использовать данный массовый процент для расчета массы растворенного вещества. Этот математический подход представлен на блок-схеме ниже:
Используя заданную плотность раствора, мы можем преобразовать объем раствора в массу, а затем использовать данный массовый процент для расчета массы растворенного вещества. Этот математический подход представлен на блок-схеме ниже:
Для правильной отмены единицы объем 0,500 л преобразуется в 500 мл, а массовый процент выражается как отношение, 37,2 г HCl / г раствора:
[латекс] \ text {раствор 500 мл} \ left (\ dfrac {1.19 \ text {g solution}} {\ text {mL solution}} \ right) \ left (\ dfrac {37.2 \ text {g HCl}} {100 \ text {g solution}} \ right) = 221 \ text {g HCl} [/ latex]
Эта масса HCl соответствует нашей приблизительной оценке примерно в 200 г.
Проверьте свои знанияВ каком объеме концентрированного раствора HCl содержится 125 г HCl?
Объем в процентах
Объемы жидкости в широком диапазоне величин удобно измерять с помощью обычного и относительно недорогого лабораторного оборудования. Концентрация раствора, образованного растворением жидкого вещества в жидком растворителе, поэтому часто выражается как объемных процентов , об. % Или (об. / Об.)%:
% Или (об. / Об.)%:
[латекс] \ text {объемный процент} = \ dfrac {\ text {объем растворенного вещества}} {\ text {объем раствор}} \ times 100 \% [/ latex]
Пример 3:
Расчеты с использованием процентного содержания объемаМедицинский спирт (изопропанол) обычно продается в виде 70% -ного водного раствора.Если плотность изопропилового спирта составляет 0,785 г / мл, сколько граммов изопропилового спирта содержится в 355-миллилитровой бутылке медицинского спирта?
Показать решениеСогласно определению процентного объема, объем изопропанола составляет 70% от общего объема раствора. Умножение объема изопропанола на его плотность дает требуемую массу:
[латекс] \ left (355 \ text {мл раствора} \ right) \ left (\ dfrac {70 \ text {мл изопропилового спирта}} {100 \ text {мл раствора}} \ right) \ left (\ dfrac { 0,785 \ text {г изопропилового спирта}} {1 \ text {мл изопропилового спирта}} \ right) = 195 \ text {г изопропилового спирта} [/ латекс]
Проверьте свои знания Вино содержит приблизительно 12% этанола (CH 3 CH 2 OH) по объему. Этанол имеет молярную массу 46,06 г / моль и плотность 0,789 г / мл. Сколько молей этанола содержится в бутылке вина объемом 750 мл?
Этанол имеет молярную массу 46,06 г / моль и плотность 0,789 г / мл. Сколько молей этанола содержится в бутылке вина объемом 750 мл?
1,5 моль этанола
Вы можете просмотреть стенограмму «Массовый процент и объемный процент — практические задачи химического состава раствора» здесь (открывается в новом окне).
Массово-объемное процентное содержание
«Смешанные» процентные единицы, полученные из массы растворенного вещества и объема раствора, популярны для определенных биохимических и медицинских применений. массово-объемный процент — это отношение массы растворенного вещества к объему раствора, выраженное в процентах. Конкретные единицы, используемые для массы растворенного вещества и объема раствора, могут варьироваться в зависимости от раствора. Например, физиологический солевой раствор, используемый для приготовления внутривенных жидкостей, имеет концентрацию 0,9% по массе / объему (м / об), что указывает на то, что состав составляет 0,9 г растворенного вещества на 100 мл раствора.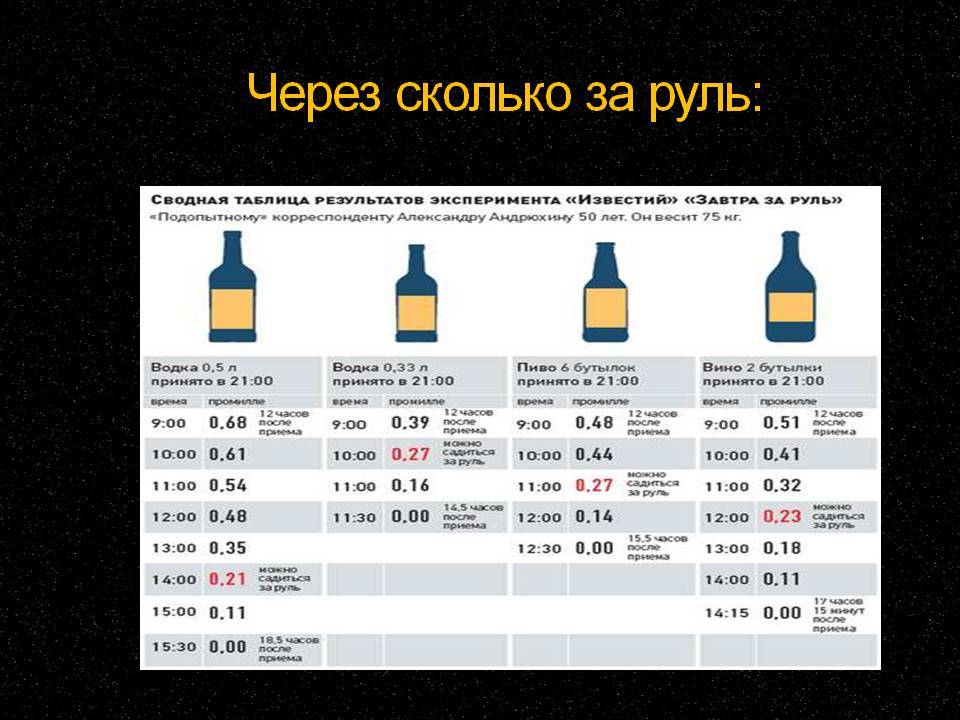 Концентрация глюкозы в крови (обычно называемая «сахар в крови») также обычно выражается в виде отношения массы к объему.Хотя его концентрация не выражается явно в процентах, его концентрация обычно выражается в миллиграммах глюкозы на децилитр (100 мл) крови (рис. 2).
Концентрация глюкозы в крови (обычно называемая «сахар в крови») также обычно выражается в виде отношения массы к объему.Хотя его концентрация не выражается явно в процентах, его концентрация обычно выражается в миллиграммах глюкозы на децилитр (100 мл) крови (рис. 2).
Рис. 2. «Смешанные» единицы массы-объема обычно встречаются в медицинских учреждениях. (а) Концентрация NaCl в физиологическом растворе составляет 0,9% (м / об). (b) Это устройство измеряет уровень глюкозы в образце крови. Нормальный диапазон концентрации глюкозы в крови (натощак) составляет около 70–100 мг / дл. (Фото a: модификация работы «Национальной гвардии» / Flickr; кредит b: модификация работы Бисварупа Гангули)
частей на миллион и частей на миллиард
Очень низкие концентрации растворенных веществ часто выражаются с использованием подходящих малых единиц, таких как частей на миллион (ppm) или частей на миллиард (ppb) .{9} \ text {ppb} [/ latex]
Как ppm, так и ppb являются удобными единицами измерения концентраций загрязняющих веществ и других микропримесей в воде. Концентрации этих загрязнителей обычно очень низкие в очищенных и природных водах, и их уровни не могут превышать относительно низкие пороговые значения концентрации, не вызывая неблагоприятных последствий для здоровья и дикой природы. Например, EPA определило, что максимально безопасный уровень фторид-иона в водопроводной воде составляет 4 ppm. Встроенные фильтры для воды предназначены для снижения концентрации фторида и некоторых других незначительных примесей в водопроводной воде (рис. 3).
Концентрации этих загрязнителей обычно очень низкие в очищенных и природных водах, и их уровни не могут превышать относительно низкие пороговые значения концентрации, не вызывая неблагоприятных последствий для здоровья и дикой природы. Например, EPA определило, что максимально безопасный уровень фторид-иона в водопроводной воде составляет 4 ppm. Встроенные фильтры для воды предназначены для снижения концентрации фторида и некоторых других незначительных примесей в водопроводной воде (рис. 3).
Рис. 3. (a) В некоторых районах следовые концентрации загрязняющих веществ могут сделать нефильтрованную водопроводную воду небезопасной для питья и приготовления пищи. (b) Встроенные фильтры для воды снижают концентрацию растворенных веществ в водопроводной воде. (кредит А: модификация работы Дженн Дарфи; кредит б: модификация работы «Вастатепаркстафф» / Wikimedia Commons)
Вы можете просмотреть расшифровку «Частей на миллион (ppm) и частей на миллиард (ppb) — Концентрация раствора» здесь (открывается в новом окне).
Пример 4:
Расчет частей на миллион и частей на миллиард концентрацийСогласно EPA, когда концентрация свинца в водопроводной воде достигает 15 частей на миллиард, необходимо принять определенные меры по исправлению положения. Что это за концентрация в промилле? Какая масса свинца (мкг) при такой концентрации содержится в типичном стакане воды (300 мл)?
Показать решениеОпределения единиц ppm и ppb могут использоваться для преобразования данной концентрации из частей на миллиард в ppm.{3} \ text {ppb}} = 0,015 \ text {ppm} [/ latex]
Определение единицы ppb может использоваться для расчета требуемой массы, если указана масса раствора. Однако указан только объем раствора (300 мл), поэтому мы должны использовать плотность, чтобы получить соответствующую массу. Мы можем предположить, что плотность водопроводной воды примерно такая же, как у чистой воды (~ 1,00 г / мл), поскольку концентрации любых растворенных веществ не должны быть очень большими. {9} \ text {ppb}} \ end {array} [ / латекс]
[латекс] \ text {масса растворенного вещества} = \ dfrac {15 \ text {ppb} \ times 300 \ text {mL} \ times \ frac {1.{-6} \ text {g}} = 4.5 \ mu \ text {g} [/ latex]
Проверьте свои знанияОбразец промышленных сточных вод массой 50,0 г содержит 0,48 мг ртути. Выразите концентрацию ртути в сточных водах в единицах ppm и ppb.
Показать решение9,6 частей на миллион, 9600 частей на миллиард
Ключевые концепции и резюме
Помимо молярности, в различных приложениях используется ряд других единиц концентрации раствора. Процентные концентрации, основанные на массе компонентов раствора, объемах или обоих, полезны для выражения относительно высоких концентраций, тогда как более низкие концентрации удобно выражать с использованием единиц ppm или ppb.{9} \ text {ppb} [/ latex]
Попробуйте
- Обдумайте вопрос: Какая масса концентрированного раствора азотной кислоты (68,0% HNO 3 по массе) необходима для приготовления 400,0 г 10,0% раствора HNO 3 по массе?
- Обрисуйте шаги, необходимые для ответа на вопрос.
- Ответьте на вопрос.
- Какая масса 4,00% раствора NaOH по массе содержит 15,0 г NaOH?
- Какая масса твердого NaOH (97.0% NaOH по массе) требуется для приготовления 1,00 л 10,0% раствора NaOH по массе? Плотность 10,0% раствора составляет 1,109 г / мл.
- Какая масса HCl содержится в 45,0 мл водного раствора HCl, который имеет плотность 1,19 г · см –3 и содержит 37,21% HCl по массе?
- Жесткость воды (количество жесткости) обычно выражается в частях на миллион (по массе) CaCO 3 , что эквивалентно миллиграмму CaCO 3 на литр воды.Какова молярная концентрация ионов Ca 2+ в пробе воды с показателем жесткости 175 мг CaCO 3 / л?
- Предполагалось, что уровень ртути в потоке превышает минимальный уровень, считающийся безопасным (1 часть на миллиард по весу). Анализ показал, что концентрация составляла 0,68 частей на миллиард. Примите плотность 1,0 г / мл и рассчитайте молярность ртути в потоке.
- В Канаде и Великобритании устройства, измеряющие уровень глюкозы в крови, выдают показания в миллимолях на литр.Если наблюдается размер 5,3 м M , какова концентрация глюкозы (C 6 H 12 O 6 ) в мг / дл?
- Горловой спрей содержит 1,40 мас.% Фенола, C 6 H 5 OH, в воде. Если раствор имеет плотность 0,9956 г / мл, рассчитайте молярность раствора.
- Йодид меди (I) (CuI) часто добавляют в поваренную соль в качестве диетического источника йода. Сколько молей CuI содержится в 1 фунте (454 г) поваренной соли, содержащей 0.0100% CuI по массе?
- Сироп от кашля содержит 5,0% этилового спирта, C 2 H 5 OH, по массе. Если плотность раствора составляет 0,9928 г / мл, определите молярность спирта в сиропе от кашля.
- D5W — раствор, используемый в качестве жидкости для внутривенного введения. Это 5,0% -ный по массе раствор декстрозы (C 6 H 12 O 6 ) в воде. Если плотность D5W составляет 1,029 г / мл, рассчитайте молярность декстрозы в растворе.
- Найдите молярность числа 40.0% по массе водный раствор серной кислоты, H 2 SO 4 , плотность которого составляет 1,3057 г / мл.
1. Ответы следующие:
- Можно использовать уравнение разбавления, соответствующим образом измененное с учетом единиц концентрации на основе массы:
[латекс] \% {\ text {масса}} _ {1} \ times {\ text {mass}} _ {1} = \% {\ text {mass}} _ {2} \ times {\ text {mass}} _ {2} [/ latex]
Это уравнение можно преобразовать так, чтобы выделить массу 1 и данные величины подставить в это уравнение .{-1} \ right) = 1029 \ text {g} \\ \ text {mol dextrose} = 1029 \ cancel {\ text {g}} \ times 0,050 \ times \ dfrac {1 \ text {mol}} {180,2 \ cancel {\ text {g}}} = 0,29 \ end {array} [/ latex][латекс] 0,29 \ text {mol C} _ {6} \ text {H} _ {12} \ text {O} _ {6} [/ latex]
Поскольку мы выбрали объем равным 1,00 л, молярность декстрозы равна [латекс] \ text {molarity} = \ dfrac {\ text {mol}} {\ text {L}} = \ dfrac {0,29 \ text {mol }} {1,00 \ text {L}} = 0,29 \ text {mol} [/ latex].
Глоссарий
массовый процент: отношение массы растворенного вещества к массе раствора, выраженное в процентах
массово-объемный процент: отношение массы растворенного вещества к объему раствора, выраженное в процентах
частей на миллиард (ppb): отношение массы растворенного вещества к раствору, умноженное на 10 9
частей на миллион (ppm): отношение массы растворенного вещества к раствору, умноженное на 10 6
объемный процент: отношение объема растворенного вещества к объему раствора, выраженное в процентах
B7: Этанол | Предельно допустимые концентрации отдельных загрязняющих веществ в воздухе для космических аппаратов: Том 3
Leichter, J., и М. Ли. 1979. Влияние материнского этанола на физический рост потомства крыс. Рост 43: 288-297.
Лестер, Д. и Л. А. Гринберг. 1951. Вдыхание человеком этилового спирта. Q. J. Stud. Алкоголь. 12: 167-178.
Либер, С. С. 1979. Патогенез и диагностика алкогольного поражения печени. Стр. 237–258 в «Метаболические эффекты алкоголя», П. Авогаро, К. Р. Сиртори и Э. Тремоли, ред. Амстердам: Эльзевир / Северная Голландия.
Либер, К.С. 1984. Алкоголь и печень: обновление 1984 года. Гепатология 4: 1243-1260.
Либер, С. С., Л. М. ДеКарли и Э. Рубин. 1975. Последовательное образование ожирения печени, гепатита и цирроза у приматов, не являющихся людьми, которых кормили этанолом с адекватной диетой. Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 72: 437-441.
Либер, С. С., Э. Бараона, М. А. Лео и А. Гарро. 1987. Метаболизм и метаболические эффекты этанола, включая взаимодействие с лекарствами, канцерогенами и питанием. Мутат. Res. 186: 201-233.
Леви, А., и Р. фон дер Хайде. 1918. Поглощение этилового спирта через дыхание [перевод]. Biochem. З. 86: 125-175.
Lowenfels, A. B. 1975. Алкоголизм и риск рака. Аня. N.Y. Acad. Sci. 252: 366-373.
Ф. Лундквист, Н. Тайгструп, К. Винклер, К. Меллемгаард и С. Мунк-Петерсен. 1962. Метаболизм этанола и производство свободного ацетата в печени человека. J. Clin. Вкладывать деньги. 41: 955-961.
Mankes, R.F., R. LeFevre, K.-F. Бениц, И. Розенблюм, Х.Бейтс, А. И. Т. Уокер, Р. Абрахам и У. Роквуд. 1982. Отцовские эффекты этанола у крысы Long-Evans. J. Toxicol. Environ. Здоровье. 10: 871-878.
Марбери, М. К., С. Линн, Р. Монсон, С. Шенбаум, П. Г. Стаблфилд и К. Дж. Райан. 1983. Связь употребления алкоголя с исходом беременности. Являюсь. J. Public Health 73: 1165-1168.
Мейсон, Дж. К. и Д. Дж. Блэкмор. 1972. Экспериментальное вдыхание паров этанола. Med. Sci. Закон 12 (3): 205-208.
Масоро, Э.Дж., Х. Абрамович и Дж. Р. Бирчард. 1953. Метаболизм C 14 -этанола в выживших тканях крысы. Являюсь. J. Physiol. 173: 37-40.
Мертенс, Х. 1896. Анатомические поражения лапчатки на основе хронического отравления хлороформом и спиртом. Arch. Int. Pharmacodyn. 2: 127.
Мюллер, Г., М. Спасовски и Д. Хеншлер. 1975. Метаболизм
.Как рассчитать концентрацию в PPM
Обновлено 9 марта 2020 г.
Ли Джонсон
Проверено: Lana Bandoim, B.S.
Когда вы работаете с растворами в химии, очень важно выразить концентрацию одного компонента по отношению ко всей смеси.
В большинстве случаев вы можете использовать более «повседневные» показатели, такие как процент, для выражения прочности смеси, но в других случаях вам понадобятся менее распространенные единицы, такие как части на миллион или PPM.
В основном это звучит так: количество частей объекта, которые вас интересуют, на каждый миллион частей решения.Но важно знать, как выполнить базовый расчет PPM, если вы собираетесь общаться с другими учеными.
Объяснение расчета PPM
Ключевым моментом PPM является то, что он сообщает вам, сколько « единиц » вещества A у вас есть на каждый миллион единиц всего раствора или смеси. Напротив, процентный показатель показывает, сколько чего-то у вас есть «на сотню», и поэтому он очень похож на PPM. Точно так же вы можете сказать, что у вас есть 7-процентное решение, вы можете сказать, что у вас есть решение на 36 PPM.
Самое важное, о чем следует помнить при выполнении расчета PPM, — это то, что единицы, которые вы выбираете для раствора, и единицы для вещества, которое вас интересует, должны совпадать. Вы не можете использовать массу растворенного вещества и объем для всего раствора, например, вы должны использовать массу и массу или объем и объем, чтобы получить ощутимый результат.
PPM в простых случаях
Есть несколько ситуаций, когда расчет PPM выполнить очень просто. Одним из них является преобразование процентного значения в значение PPM, потому что 1 PPM всего в 10 000 раз больше, чем один процент.Затем, чтобы выполнить преобразование, просто умножьте значение в процентах на 10 000 или 10 4 . Например, если у вас 0,02-процентный раствор, это эквивалентно 0,02 × 10 4 = 200 частей на миллион, что для является гораздо более удобной цифрой , чем крошечный процент.
Еще один простой пример — это редкий случай, когда можно легко смешивать массы и объемы и конвертировать в PPM. Поскольку 1 литр воды имеет массу 1 кг, любая концентрация, выраженная в мг / л, равна уже в PPM, потому что это эквивалентно мг / кг.Так что, если у вас есть смесь 132 мг / л, то это 132 частей на миллион, и вы даже можете выполнять простые преобразования из таких вещей, как г / л в PPM, используя этот факт (просто преобразуйте массу в мг, и все готово).
Общая формула для PPM
В целом, однако, вы всегда можете рассчитать PPM, используя один подход и простую формулу . Первое, что вам нужно сделать, это измерить количество растворенного вещества или вещества, которое вас интересует, а затем провести такое же измерение для всего раствора, например.6
Вы можете разбить его на двухэтапный процесс, если это поможет: во-первых, разделите количество растворенного вещества на количество всего раствора, чтобы получить измерение концентрации «частей на 1».
С этого момента вы просто умножаете его на 1000000, чтобы преобразовать его в измерение PPM, или, альтернативно (если это лучше подходит для концентрации, с которой вы работаете), вы можете умножить на 100, чтобы преобразовать его в процент, или 1000000000, чтобы превратить его в значение частей на миллиард (PPB).Просто помните, что вам нужно сохранить те же единицы измерения, и процесс прост.
Высокоселективное обнаружение метанола по сравнению с этанолом ручным датчиком газа
Конструкция детектора
На Рисунке 1а показан портативный детектор метанола. Он состоит из разделительной колонны перед микромашинным датчиком газа на основе оксида металла, размещенным внутри тефлоновой камеры. Дыхание или свободное пространство напитка можно втянуть насосом через разделительную колонку к датчику. Разделительная колонка представляет собой миниатюрную колонку для ГХ с Tenax TA в качестве стационарной фазы (показана на рис.1б) с более низкой прочностью адсорбции метанола по сравнению с этанолом 23 . На рисунке 1с показано изображение поверхности частицы Tenax, полученное с помощью сканирующей электронной микроскопии (СЭМ), показывающее ее высокую удельную поверхность (35 мкм 2 г -1 ) и пористость (средний размер пор 200 нм). По сравнению с типичными колонками для ГХ 22 , используемая здесь разделительная колонка намного короче (4,5 см) и толще (внутренний диаметр 4 мм). Вместе с небольшим количеством используемого адсорбента (150 мг) и его большим размером частиц (~ 200 мкм) это приводит к достаточно небольшому перепаду давления (<20 мбар) для обеспечения требуемой скорости потока (25 мл мин. -1 ) к датчику.
На рис. 1d показан датчик, закрепленный на держателе микросхемы. Он изготовлен на микромашиностроении, отличается небольшими размерами и минимальной потребляемой мощностью (76 мВт при 350 ° C), легко подходит для интеграции в портативное устройство. На рис. 1e, f показаны СЭМ-изображения сверху чувствительной пленки, изготовленной из хеморезистивных наночастиц SnO, легированного палладием 2 наночастиц 26 , обладающих высокой пористостью и удельной площадью поверхности (~ 80 м 2 г -1 для приготовленных аналогичным образом SnO, легированный платиной 2 ) 27 .Открытая пленочная структура обеспечивает быструю диффузию аналитов и взаимодействие с большой площадью поверхности, что важно для быстрого и высокочувствительного определения метанола. Такие датчики использовались, например, для обнаружения формальдегида всего 3 частей на миллиард с быстрым откликом (140 с) и временем восстановления (190 с), а также хорошей воспроизводимостью (отклонение отклика <10%) 28 .
Селективное обнаружение метанола
На рис. 2а показаны отклики датчика SnO, легированного палладием 2 без разделительной колонки, на 10-секундное воздействие 5 ppm водорода (фиолетовая линия), метанола (красная линия), ацетона (зеленая линия) и этанол (синяя линия) при относительной влажности 50%.Датчик быстро реагирует на все эти аналиты с ответами от 10 до 25. Однако он не может различить их. Это становится еще более очевидным при воздействии на сенсор смеси этих аналитов (рис. 2b). Сенсор теперь дает гораздо более высокий отклик, немного ниже, чем сумма отдельных откликов, что обычно наблюдается для хеморезистивных сенсоров при таких концентрациях ppm 29 . Как следствие, этот датчик не может избирательно измерять метанол в присутствии таких помех.
Рис. 2Ответы на отдельные и смешанные аналиты без и с разделительной колонкой. Отклик детектора метанола a , b без и c , d с разделительной колонкой на 10-секундные воздействия 5 ppm водорода (фиолетовая линия), метанола (красная линия), этанола (синяя линия) и ацетон (зеленая линия), а также их смесь (черная линия в b и d ) при относительной влажности 50% и общей скорости потока не менее 25 мл -1 . Также приведены соответствующие времена удерживания ( t R , пунктирные линии, для водорода t R = 0 мин, поскольку он не удерживается).Обратите внимание на различную шкалу ординат между a , b и c , d . Наличие уплотненного слоя полимерного сорбента перед датчиком SnO, легированным палладием 2 , способствует разделению компонентов смеси.
В сочетании с разделительной колонкой отклики датчика разделяются, как в хроматографе. Отклик на водород (фиолетовая линия) остается прежним (рис. 2в). Это ожидается, поскольку водород имеет низкую молекулярную массу и не удерживается Tenax 30 .Однако для других аналитов наблюдается иное поведение. Фактически, метанол (красная линия) теперь обнаруживается через> 1 мин с максимальным откликом сенсора (т.е. время удерживания t R , пунктирные линии) через 1,7 мин. Обратите внимание, что максимальная реакция на метанол ниже, чем без разделительной колонки, поскольку колонка рассеивает его в течение более длительного периода времени, в соответствии с теорией 31 . Наиболее важно, что этанол (синяя линия, т R = 8,7 мин) и ацетон (зеленая линия, т R = 33 мин) сохраняются гораздо дольше, что согласуется с литературными данными ( т R = 2.2, 10,8 и 36 мин для метанола, этанола и ацетона соответственно при 20 ° C) 30 . В результате разделительная колонка обеспечивает селективное обнаружение метанола. Интересно также, что реакции этанола и ацетона уменьшаются с увеличением t R . Фактически, реакция на 5 ppm ацетона почти не улавливается сенсором (в то время как она была вдвое выше, чем у метанола без разделительной колонки, сравните Рис. 2a, c).
При воздействии на сенсор с разделительной колонкой смеси тех же аналитов и концентраций (рис.2d), аналиты могут быть обнаружены индивидуально при их определенном времени удерживания с очень высокой селективностью, идентичной воздействиям одного аналита (рис. 2c). Наиболее примечательно, что для целевых приложений метанол обнаруживается без вмешательства этанола, что превосходит современные датчики метанола, где самая высокая селективность по этанолу (> 30) была зарегистрирована для отпечатанного Ag, легированного LaFeO 3 core- частицы оболочки 32 .
Как показано на рис. 2c, d, детектор полностью восстанавливается после каждого воздействия аналита или смеси путем продувки воздухом.Время восстановления зависит от анализируемого вещества и примерно в два-три раза превышает время удерживания в соответствии с литературными данными 33 . Время восстановления можно значительно уменьшить, просто увеличив скорость потока или слегка нагревая разделительную колонку (например, ацетон с ~ 60 мин до 20 с 30 при кратковременном увеличении температуры колонки и скорости потока до 80 ° C и 100 мл мин −1 ) 23 .
Динамический диапазон
Концентрация метанола в целевых приложениях может составлять от нескольких частей на миллион в выдыхаемом воздухе 10 до нескольких сотен частей на миллион в свободном пространстве напитков 34 .На рис. 3 показан отклик сенсора SnO 2 , легированного палладием, с разделительной колонкой при воздействии в течение 10 с 1–918 частей на миллион метанола при относительной влажности 50%. Также показаны средняя концентрация метанола в здоровом дыхании 35 (зеленая линия) и диапазон экзогенных концентраций 36 (оранжевая линия) и токсичного метанола в выдыхаемом воздухе 1 (красная область). Кривая отклика является нелинейной в соответствии с теорией диффузионных реакций 29 для таких полупроводниковых пленок из оксидов металлов при высоких концентрациях аналита.Тем не менее, в результате эта разделительная колонка-сенсорная система может отличать явно токсичные уровни от нетоксичных и даже обнаруживать низкие концентрации 1 ppm с отношением сигнал / шум> 100. Более низкие концентрации не имеют отношения к анализу свободного пространства щелока и дыхания, но такие газовые сенсоры SnO 2 , легированные палладием, могут обнаруживать летучие органические соединения вплоть до уровней единичных частей на миллиард (например, 3 частей на миллиард формальдегида 28 ). Напротив, другие настольные детекторы метанола (например, PTR-TOF-MS) также могут обнаруживать такие низкие концентрации, но они имеют гораздо меньший динамический диапазон и требуют разбавления для измерения высоких концентраций ppm, присутствующих в выдыхаемом воздухе или в свободном пространстве напитков.
Рис. 3Динамический диапазон детектора. Отклик детектора (разделительная колонка Tenax + датчик SnO 2 , легированный палладием) на концентрации метанола 1–918 ppm (черные квадраты и пунктирная линия). Показана средняя концентрация метанола в дыхании для здорового дыхания 35 (зеленая пунктирная линия), экзогенного 36 (оранжевая пунктирная линия) и токсичного 1 (красная пунктирная линия и заштрихованная область). Измерения проводились с 10-секундной экспозицией всех концентраций метанола при относительной влажности 50% и скорости потока 25 мл мин. -1 через детектор
Обратите внимание, что кривая отклика на рис.3 действительно для температуры разделительной колонки 22 ° C при относительной влажности 50%. С увеличением температуры колонки отклики сенсора становятся выше, поскольку t R уменьшается (дополнительный рис. 1a). Однако наиболее важно то, что метанол четко отделяется и детектируется отдельно от этанола даже при 40 ° C. Такие температурные эффекты могут быть учтены датчиком температуры. При более высокой влажности t R не изменяется, в соответствии с литературными данными 23 , но отклики уменьшаются (дополнительный рис.1б). Это типично для таких легированных датчиков SnO 2 20 и может быть решено путем использования материала датчика, менее чувствительного к влажности (например, SnO, легированного сурью 2 37 ) или путем корректировки с помощью датчика влажности, как это сделано. с матрицами датчиков для контроля выбросов летучих веществ из дыхания и кожи человека 38 .
Высокий фон этанола
Для анализа метанола в свободном пространстве алкогольных напитков или в состоянии алкогольного опьянения детектор должен сохранять точность в присутствии очень высоких концентраций этанола.На рисунке 4a показан отклик детектора при воздействии метанола 1 ppm с мешающими концентрациями этанола 5 (зеленая линия), 650 (относительное насыщение 1%, синяя линия) и 32 500 ppm (относительное насыщение 50%, красная линия). Несмотря на значительно более высокую концентрацию этанола, метанол обнаруживается первым ( t R = 1,5–1,7 мин), что дает сопоставимые результаты при калибровке одним газом (рис. 3). Этанол обнаруживается позже со временем прорыва ( t B , пунктирные линии), которое уменьшается с увеличением концентрации (5.От 7 мин при 5 ppm до 2,2 мин при 50% насыщении), но всегда выше, чем t R метанола. В ГХ такое же явление наблюдается при перегрузке колонки аналитом 39 .
Рис. 4Обнаружение метанола с высокой интерференцией этанола. a Отклики метанольного детектора при воздействии 1 ppm метанола в присутствии 5 (зеленая линия), 650 (относительное насыщение 1%, синяя линия) и 32 500 ppm (относительное насыщение 50%, красная линия) этанола.Соответствующие времена прорыва этанола ( t B , пунктирные линии) указаны. b Этанол t B (квадраты и пунктирная линия) и время удерживания метанола ( t R , кружки и сплошная линия) как функция мешающей концентрации этанола 5 (зеленый), 650 (1 % относительной насыщенности, синий), 6500 (относительная насыщенность 10%, оранжевый), 32500 ppm (относительная насыщенность 50%, красный) и 62000 ppm (относительная насыщенность 95%, фиолетовый)
Интересно, что при концентрации насыщения этанолом 50%, метанол обнаруживается несколько раньше с более высоким максимумом пика и меньшей шириной.Вероятно, это связано с конкурентной адсорбцией на Tenax, где метанол замещается этанолом, который адсорбирует сильнее 40 . Тем не менее, результирующая ошибка в 17% достаточно мала для целевых применений, поскольку разница между нормальными и токсичными концентрациями метанола в ликворе и дыхании намного больше (например, медиана дыхания человека 0,46 ppm 35 по сравнению с интоксикацией> 133 ppm 1 ). Если требуется более высокая точность, в качестве альтернативы можно оценить область ниже метанольного отклика, как это обычно делается в газовой хроматографии 22 .Фактически, площади пиков ниже откликов метанола в основном идентичны (в пределах 2%), независимо от концентрации этанола (дополнительный рисунок 2).
Что наиболее важно, реакция метанола четко отделена от реакции этанола даже при очень высоких концентрациях. Это показано на рис. 4b, где t R метанола (сплошная линия) и t B этанола (пунктирная линия) нанесены на график для концентраций этанола в диапазоне 5–62 000 ppm (95% насыщенность). t B экспоненциально уменьшается с увеличением концентрации, что соответствует литературным данным при более низких концентрациях 31 . Даже в самых экстремальных условиях 95% насыщенной атмосферы этанола метанол обнаруживается независимо от этанола, поскольку его реакция четко отделена от прорыва этанола. Эти результаты поразительны, учитывая простоту этого устройства, и превосходят другие детекторы метанола.
Алкоголь и дыхание с добавлением метанола
Употребление всего лишь 6 мл метанола может быть фатальным 41 .Таким образом, детектор метанола для проверки алкогольных напитков может помочь предотвратить вспышки отравления метанолом. Порог безопасности для встречающегося в природе метанола в щелоке (40 об.% Этанола) составляет 0,4 об.% (US 34 и EU 36 ), поскольку такие низкие уровни являются побочным продуктом ферментации 34 . Поэтому детектор должен уметь отличать «безопасные» алкогольные напитки от испорченных, обычно с гораздо более высоким содержанием метанола. На рис. 5а показаны ответы на чистый (зеленая линия) и с добавлением аррака (распространенный ликер в Юго-Восточной Азии) с 0.3 (синяя линия), 0,4 (оранжевая линия), 0,5 (фиолетовая линия) и 1 об.% (Красная линия) метанола. Детектор четко распознает добавленный метанол при ожидаемых t R = 1,7 мин, что соответствует времени удерживания метанола в лабораторных газовых смесях (рис. 2c и 4).
Рис. 5Обнаружение метанола в щелочной смеси (Arrack). a Отклик детектора на чистый щелок (зеленая линия), содержащий 40 об.% Этанола и добавленный метанолом 0,3 (синяя линия), 0.4 (оранжевая линия), 0,5 (фиолетовая линия) и 1 об.% (Красная линия). b Отклики сенсора в зависимости от содержания метанола (0–10 об.%) В щелоке (черные кружки). Красная пунктирная линия указывает на разрешенное законом (US 34 и EU 36 ) содержание природного метанола в щелоке (40 об.% Этанола). Планки погрешностей указывают на стандартное отклонение по крайней мере трех измерений (т. Е. Повторяемость) с отклонением <15%
Что наиболее важно, отклик увеличивается с увеличением концентрации метанола и даже небольшими различиями между 0.3, 0,4 и 0,5 об.% (Т.е. близко к допустимому пределу) могут быть четко определены датчиком с высоким отношением сигнал / шум> 100. Во всех случаях реакция резко возрастает через 3 мин, что соответствует высокой концентрации этанола. Также при более высоком содержании метанола 5 и 10 об.% Чувствительность сенсора продолжает увеличиваться (рис. 5b). В результате детектор метанола может четко отличить чистый Arrack от детектора с токсичными уровнями метанола с хорошей воспроизводимостью (отклонение <15%, погрешности на рис.5б). Из-за высокого отношения сигнал / шум также должны обнаруживаться более низкие концентрации метанола, что может быть интересно для мониторинга производства и контроля качества алкогольных напитков (например, встречающийся в природе метанол в вине 42 ).
Детектор метанола также отличается хорошей стабильностью с дрейфом базовой линии датчика 0,7% в день в течение 18 дней тестирования (дополнительный рисунок 4). Такие отклонения можно исправить дополнительным алгоритмом обработки 43 .Путем продувки окружающим воздухом он полностью регенерируется в течение 15 минут (дополнительный рисунок 3a), что позволяет проводить быстрый скрининг и многократное использование без наблюдаемых эффектов насыщения или деградации в течение как минимум 2 недель повторных испытаний (дополнительный рисунок 4).
В качестве подтверждения концепции анализа дыхания мы оценили детектор метанола на исходном дыхании с добавлением метанола у отравленного (после приема этанола) добровольца (уровень алкоголя в крови 0,54 ‰, измеренный с помощью Dräger Alcotest).Отравление добровольцев метанолом недопустимо. Однако добавление анализируемого вещества к образцу (т. Е. Метод стандартного добавления 44 ) является стандартным подходом в аналитической химии, поскольку сохраняется сложность газовой матрицы (т. Е. Отравленное дыхание). На рисунке 6а показан отклик детектора для нормального дыхания (синяя пунктирная линия) и дыхания с добавлением метанола (135 ppm метанола, красная сплошная линия). Обратите внимание, что была выбрана концентрация метанола 135 ppm, поскольку она чуть выше порога серьезной интоксикации метанолом (> 133 ppm 1 ).В обоих случаях детектор показывает идентичные отклики на водород при t = 0–30 с (не удерживается) и этанол ( t R = 8,3 мин) с последующим полным восстановлением (дополнительный рис. 3b). Четкий пик, связанный с метанолом, виден при t R = 1,7 мин с высоким отношением сигнал / шум (> 1000), идентичным лабораторным газовым смесям (рис. 2c). Для проверки пиков метанола (фиг. 6b) и этанола (фиг. 6c) одни и те же пробы выдыхаемого воздуха анализировали с помощью настольного PTR-TOF-MS, оборудованного той же разделительной колонкой.Обратите внимание, что эти высокие концентрации можно было измерить только с помощью PTR-TOF-MS путем дополнительного разбавления (см. Методы). Метанол и этанол были обнаружены при т R , идентичных датчику, что подтверждает результаты датчика.
Рис. 6Обнаружение метанола при импульсном дыхании. a Реакция детектора метанола на дыхание отравленного добровольца (уровень алкоголя в крови 0,54 ‰), взятое из мешков Тедлара. Синяя пунктирная линия показывает измерение для образца нормального дыхания, а красная сплошная линия — для образца с добавкой метанола 135 ppm, что указывает на интоксикацию метанолом.Измерения PTR-TOF-MS (с разделительной колонкой и разбавлением) тех же образцов для b метанола и c этанола. Прибор, показанный в c , представляет собой PTR-TOF-MS 1000 (Ionicon, Австрия), используемый для проверки датчика. Водород (H 2 ) не задерживается разделительной колонкой и не мешает работе детектора метанола.
В результате этот детектор может четко различать нормальное дыхание и дыхание с добавлением метанола. Следовательно, это перспективно для быстрого и неинвазивного определения отравления метанолом.Учитывая высокое отношение сигнал / шум при 135 ppm метанола, это также показывает перспективу для мониторинга удаления метанола во время обработки 10 . Конечно, результаты являются довольно предварительными (протестирован только один субъект), и требуется дальнейшая проверка на расширенных когортах, как это было недавно сделано с ацетоном для дыхания и аналогичным датчиком (Si-допированный WO 3 ) для мониторинга сжигания жира во время упражнений 45 и диета 46 .
Интересно, что спиртные напитки (рис. 5) и дыхание человека (рис.6), датчик четко определяет только метанол, этанол и водород (дыхание), хотя и щелок 47 , и выдох 48 представляют собой сложные смеси, содержащие более 100 и 800 аналитов соответственно. Вероятно, это происходит из-за более высокой молекулярной массы и различных функциональных групп (например, диолов или гликолей) большинства мешающих веществ, что приводит к более длительному удерживанию в разделительной колонке, чем метанол (например, этиленгликоль в 100 раз дольше, чем метанол 30 ). Однако наиболее вероятной причиной является гораздо более низкая концентрация большинства искажающих факторов (например,г., 0,003 ppm триметиламина в выдыхаемом воздухе 49 по сравнению с> 133 ppm метанола в случае интоксикации 1 ).
Насколько нам известно, это первый датчик метанола для определения соответствующих концентраций в присутствии этанола в реальных образцах ликвора и выдыхаемого воздуха. Другие датчики представляют собой либо жидкостные датчики, которые нельзя использовать для дыхания (например, металлоорганический каркасный датчик на основе фотолюминесцентного Tb 3+ 50 ), которые не обеспечивают требуемый предел обнаружения (например,g., кварцевый датчик на основе камертона 51 ) или не тестировались в газовых смесях (например, оптоволоконный датчик 52 ).
Содержание алкоголя в крови — wikidoc
Содержание алкоголя в крови (BAC) или Концентрация алкоголя в крови — это концентрация алкоголя в крови. Обычно это измеряется как масса на объем. Например, BAC 0,02% означает 0,02 грамма алкоголя на 100 граммов крови человека или 0,2 грамма алкоголя на 1000 граммов крови.Концентрация алкоголя в крови измеряется в таком большом количестве различных единиц, что это может сбивать с толку. Следующая формула может помочь.
Уровни алкоголя в крови
1 г / кг = 1 г кг -1 = 1 г / л = 100 мг / дл = 1 мг / куб.см = 100 мг% = 1 дециграмм% = 0,1 г% = 0,1%
Во многих странах BAC измеряется и сообщается как грамма алкоголя на 1000 миллилитров (1 литр) крови (г / 1000 мл). Поскольку удельный вес крови очень близок к удельному весу воды (ее основного компонента), числовые значения для BAC (%, проценты) и (г / 1000 мл, промилле) не отличаются ни в какой степени, кроме размещение десятичной точки.
В Великобритании BAC выражается в миллиграммах алкоголя на 100 миллилитров крови. Например, BAC 0,08% законодательно установлен как предел 80 мг на 100 мл [1]. Он также указывается в граммах на литр, что является эквивалентным измерением [2].
Количество выпитых напитков — очень плохой показатель опьянения, в основном из-за различий в физиологии и индивидуальной переносимости алкоголя. Тем не менее, общепринято, что употребление в трезвом виде двух стандартных напитков (содержащих в общей сложности 20 граммов) алкоголя увеличивает BAC в среднем человека примерно на 0.05% (один стандартный напиток, потребляемый каждый час после первых двух, будет поддерживать BAC примерно на уровне 0,05%), но есть большие различия в зависимости от массы тела, пола и процентного содержания жира в организме. Кроме того, ни BAC, ни количество выпитых напитков не обязательно являются точными показателями уровня нарушения. Толерантность к алкоголю варьируется от человека к человеку и может зависеть от таких факторов, как генетика, адаптация к хроническому употреблению алкоголя и синергетические эффекты наркотиков.
Содержание алкоголя в крови можно непосредственно измерить в больничной лаборатории.Чаще всего в расследованиях правоохранительных органов BAC оценивается по концентрации алкоголя в выдыхаемом воздухе (BrAC), измеренной с помощью устройства, обычно называемого алкотестером, который является универсальной торговой маркой.
Эффекты на разных уровнях
Шаблон: См. Также Если у человека не разовьется высокая толерантность, рейтинг BAC 0,20 представляет очень серьезное опьянение (большинство пьющих впервые теряют сознание примерно к 0,15), а 0,35 означает потенциально смертельное отравление алкоголем.0,40 — это принятая LD 50 , или летальная доза для 50% взрослых людей. Для тех, кто много пьет, эти цифры могут как минимум удвоиться. В крайних случаях люди пережили рейтинг BAC до 0,914.
Прогрессирующие эффекты алкоголя [1] BAC Поведение Обесценение .01 – .06 - Отдых
- Чувство благополучия
- Потеря ингибирования
- Пониженная бдительность
- Радостный
- Мысль
- Решение
- Координация
- Концентрация
.06 – .10 - Притупленные чувства
- Растормаживание
- Экстраверсия
- Нарушение сексуального удовольствия
- Нарушены рефлексы
- Рассуждения
- Восприятие глубины
- Расстояние Acuity
- Периферийное зрение
- Устранение бликов
.11 – .20 - Чрезмерное выражение
- Эмоциональные качели
- Злой или грустный
- Шумный
- Время реакции
- Полный контроль двигателя
- Потрясающе
- Невнятная речь
.21–,29 - Ступор
- Терять понимание
- Нарушенные ощущения
- Серьезное повреждение мотора
- Потеря сознания
- Отключение памяти
.30– .39 - Тяжелая депрессия
- Без сознания
- Возможна смерть
- Функция мочевого пузыря
- Дыхание
- ЧСС
>.40 Таблица стандартных напитков [2] Шаблон: См. Также Спирт Количество в мл Сумма в эт. унция. Разговорная сумма Крепкий ликер 80 37 миллилитров 1,25 унции один маленький выстрел пиво 355 миллилитров 12 унций одна банка вино столовое 148 миллилитров 5 унций один маленький стакан Мужской
ЖенскийПриблизительное процентное содержание алкоголя в крови [3] Напитки Масса тела 40 кг 45 кг 55 кг 64 кг 73 кг 82 кг 91 кг 100 кг 109 кг 90 фунтов 100 фунтов 120 фунтов 140 фунтов 160 фунтов 180 фунтов 200 фунтов 220 фунтов 240 фунтов 1 —
.05.04
.05.03
.04.03
.03.02
.03.02
.03.02
.02.02
.02.02
.022 –
.10.08
.09.06
.08.05
.07.05
.06.04
.05.04
.05.03
.04.03
.043 –
0,15.11
.14.09
.11.08
.10.07
.09.06
.08.06
.07.05
.06.05
.064 —
,20,15
,18.12
.15.11
.13.09
.11.08
.10.08
.09.07
.08.06
.085 –
.25,19
,23,16
,19,13
,16.12
.14.11
.13.09
.11.09
.10.08
.096 –
. 30,23
,27,19
,23,16
,19,14
.17,13
,15.11
.14.10
.12.09
.117 —
,35,26
,32,22
,27,19
,23,16
,20,15
,18,13
,16.12
.14.11
.138 –
.40,30
,36,25
.30,21
,26,19
,23,17
,20,15
,18,14
,17,13
,159 –
. 45,34
,41,28
,34,24
,29,21
,26,19
,23,17
,20,15
,19,14
,1710 —
.51,38
,45,31
,38,27
,32,23
,28,21
,25,19
,23,17
,21,16
,19Вычитайте примерно 0,01% каждые 40 минут после питья. Чтобы использовать простой калькулятор содержания алкоголя в крови от Департамента общественной безопасности штата Висконсин, перейдите по следующей ссылке: Калькулятор содержания алкоголя в крови
Единицы измерения
В мире существует несколько различных единиц измерения концентрации алкоголя в крови.Каждый определяется как масса алкоголя на единицу объема крови или масса алкоголя на массу крови (но не как объем на единицу объема). 1 миллилитр крови приблизительно эквивалентен 1 грамму крови, а если быть точным, 1,06 грамма. Из-за этого единицы по объему похожи, но не идентичны единицам по массе.
Блок Размеры Эквивалент Используется в 1 процент BAC по объему 1/100 (%) г / мл = 1 мкг / мл 9.43 мг / г, 0,217 ммоль / л Соединенные Штаты 1 промилле BAC по объему 1/1000 (‰) г / мл = 1 мг / мл 0,943 мг / г, 0,0217 ммоль / л Нидерланды, Литва, Польша 1 базисный пункт BAC по объему 1/10 000 (шаблон: Unicode) г / мл = 100 Шаблон: Unicodeg / мл 94,3 ppm, 2,17 Шаблон: Unicodemol / L Великобритания 1 промилле BAC по массе 1/1000 (‰) г / г = 1 мг / г 1.06 мг / мл, 0,0230 ммоль / л Финляндия, Норвегия, Швеция 1 часть на миллион 1/1000000 (ppm) г / г = 1 Шаблон: Unicodeg / g 1.06 Шаблон: Unicodeg / mL, 0,0230 Шаблон: Unicodemol / L 1 тысячная Молярность 1 ммоль / л 4,6 cg / мл, [4] 4,34 cg / g Медицинский персонал Юридические ограничения
В правоохранительных органах BAC используется для определения интоксикации и дает приблизительную оценку степени обесценения.Хотя степень нарушения может быть разной у людей с одним и тем же BAC, ее можно объективно измерить, и поэтому она полезна с юридической точки зрения, и ее трудно оспорить в суде. В большинстве стран запрещена эксплуатация автотранспортных средств и тяжелой техники с превышением установленного уровня BAC. Также регулируется эксплуатация лодок и самолетов.
Ограничения по странам (BAC: содержание алкоголя в крови)
Уровень алкоголя, при котором человек считается инвалидом, зависит от страны. В приведенном ниже списке указаны ограничения по странам.Обычно это пределы BAC (содержания алкоголя в крови) для эксплуатации транспортного средства.
Ограничения по странам (BrAC: содержание алкоголя в выдыхаемом воздухе)
В некоторых странах лимиты алкоголя определяются содержанием алкоголя в выдыхаемом воздухе (BrAC), не путать с BAC.
- В Греции предел BrAC составляет 25 микрограммов алкоголя на 1000 миллилитров выдыхаемого воздуха. Предел в крови 0,50 г / л).
- В Нидерландах и Финляндии предел BrAC составляет 220 микрограммов алкоголя на литр дыхания (мкг / л, в просторечии известный как «угл»).
Другие схемы ограничения
- Для Южной Кореи штрафы за разные уровни BAC включают
- 0,01–0,049 = без штрафа
- 0,05–0,09 = 100 дней аннулирования лицензии
- > 0,10 = Аннулирование лицензии на автомобиль.
- > 0,36 = арест
- Быть пойманным за рулем в нетрезвом виде 3 раза за 5 лет; или 2 раза в 3 года приводит к аресту.
Тестовые допущения
Тесты на содержание алкоголя в крови предполагают, что тестируемый человек имеет средние показатели по различным параметрам.Например, в среднем отношение BAC к содержанию алкоголя в выдыхаемом воздухе (коэффициент распределения ) составляет 2100: 1. Другими словами, на каждую часть вдоха в крови приходится 2100 частей алкоголя. Однако фактическое соотношение у любого конкретного человека может варьироваться от 1300: 1 до 3100: 1 или даже более широко. Это соотношение меняется не только от человека к человеку, но и внутри одного человека от момента к моменту. Таким образом, человек с истинным уровнем алкоголя в крови 0,08, но с коэффициентом распределения 1700: 1 во время тестирования будет иметь.10 показаний алкотестера, откалиброванного для среднего соотношения 2100: 1.
Аналогичное предположение делается при анализе мочи. Когда моча анализируется на алкоголь, предполагается, что на каждую часть крови в моче приходится 1,3 части алкоголя, хотя фактическое соотношение может сильно варьироваться.
Тестирование на алкоголь в выдыхаемом воздухе также предполагает, что тест пост-абсорбционный — то есть, что абсорбция алкоголя в организме субъекта завершена. Если субъект все еще активно поглощает алкоголь, его тело не достигло состояния равновесия , при котором концентрация алкоголя одинакова по всему телу.Большинство судебно-медицинских экспертов по алкоголю отвергают результаты тестов в этот период, поскольку количество алкоголя в выдыхаемом воздухе не будет точно отражать истинную концентрацию в крови.
Метаболизм и выведение
Алкоголь удаляется из кровотока в результате метаболизма, выведения и испарения. Относительная доля утилизируемых в том или ином виде варьируется от человека к человеку, но обычно от 90 до 98% метаболизируется, от 1 до 3% выводится с мочой и от 1 до 5% испаряется с дыханием.Очень небольшая часть (менее 0,5%) также выводится с потом, слезами и т.д. мозг. (Фактически, у некоторых мужчин уровни алкогольдегидрогеназы в желудке достаточно высоки, чтобы некоторый метаболизм происходил даже за до того, как алкоголь всасывается за ).
Метаболизм в основном осуществляется группой из шести ферментов, вместе называемых алкогольдегидрогеназой.Они превращают этанол в ацетальдегид (промежуточный продукт, который на самом деле более токсичен, чем этанол). Затем фермент ацетальдегиддегидрогеназа превращает ацетальдегид в нетоксичный ацетил-КоА.
Многие физиологически активные вещества удаляются из кровотока (метаболизмом или экскрецией) со скоростью, пропорциональной текущей концентрации, так что они демонстрируют экспоненциальный распад с характерным периодом полураспада (см. Фармакокинетика). Однако это не относится к алкоголю.Обычные дозы алкоголя фактически насыщают ферменты, так что алкоголь удаляется из кровотока примерно с постоянной скоростью. Этот показатель значительно варьируется между людьми; опытные пьющие мужчины с высокой массой тела могут перерабатывать до 30 граммов (38 мл) в час, но более типичная цифра составляет 10 граммов (12,7 мл) в час. Лица моложе 25 лет, женщины, лица определенных этнических групп и люди с заболеваниями печени могут перерабатывать алкоголь медленнее. Многие выходцы из Восточной Азии (т.е.г. около половины японцев) имеют нарушенную ацетальдегиддегидрогеназу; это приводит к повышению пикового уровня ацетальдегида, вызывая более тяжелое похмелье и другие эффекты, такие как приливы крови к лицу и тахикардия. И наоборот, представители определенных этнических групп, которые традиционно не варили алкогольные напитки, имеют более низкий уровень алкогольдегидрогеназ и, таким образом, «протрезвевают» очень медленно, но достигают более низких концентраций альдегидов и имеют более легкое похмелье. Скорость детоксикации алкоголя также может быть замедлена некоторыми лекарствами, которые препятствуют действию алкогольдегидрогеназ, особенно аспирин, фурфурол (который может быть найден в сивушном масле), пары определенных растворителей, многие тяжелые металлы и некоторые соединения пиразола.Также подозревают, что на этот эффект оказывают циметидин (Тагамет), ранитидин (Зантак) и ацетаминофен (Тайленол).
В настоящее время нет известных лекарств или других веществ, которые можно принимать внутрь, которые ускоряют метаболизм алкоголя. Прием алкоголя можно замедлить, приняв его на полный желудок. Алкоголь из негазированных напитков всасывается медленнее, чем алкоголь из газированных напитков.
Ретроградная экстраполяция — это математический процесс, с помощью которого определяется концентрация алкоголя в крови человека во время вождения путем проецирования назад результатов более позднего химического теста.Это включает оценку абсорбции и выведения алкоголя в промежутке между вождением и тестированием. Скорость элиминации у среднего человека обычно оценивается от 0,015 до 0,020 процента в час, хотя, опять же, она может варьироваться от человека к человеку и от одного человека к другому. На метаболизм может влиять множество факторов, включая такие факторы, как температура тела, тип потребляемого алкогольного напитка, а также количество и тип потребляемой пищи.
Во все большем числе штатов принимаются законы, облегчающие эту умозрительную задачу: BAC во время вождения юридически считается таким же, как и при последующих испытаниях.На это предположение обычно устанавливаются временные рамки, обычно два или три часа, и обвиняемому разрешается представить доказательства, опровергающие это предположение.
Также может быть предпринята прямая экстраполяция. Если известно количество выпитого алкоголя, а также такие переменные, как вес и пол пациента, период и скорость потребления, уровень алкоголя в крови можно оценить путем экстраполяции вперед. Несмотря на те же недостатки, что и ретроградная экстраполяция — предположения, основанные на средних значениях и неизвестных переменных — это может иметь значение для оценки BAC при вождении и / или подтверждения или опровержения результатов более позднего химического теста.
Расчет содержания алкоголя в крови
BAC можно приблизительно оценить с помощью математического подхода. Хотя математическая оценка BAC не так точна, как алкотестер, она может быть полезна для расчета уровня BAC, который в настоящее время не поддается проверке, или уровня, который может присутствовать в будущем. Хотя существует несколько способов расчета BAC, один из наиболее эффективных — просто измерить общее количество потребляемого алкоголя, разделенное на общее количество воды в организме, что фактически дает процент алкоголя на объем воды в крови.
Общий вес воды человека можно рассчитать, умножив вес его тела на процент воды. Например, у женщины весом 150 фунтов общее количество воды составит 73,5 фунта (150 x 0,49). Для простейших расчетов этот вес должен быть в килограммах, который можно легко преобразовать, разделив общую сумму фунтов на 2,205. 73,5 фунта воды эквивалентны 29,4 кг воды. 29,4 кг воды эквивалентны 29 400 мл воды (1 л воды весит 1 кг, а 1 л = 1000 мл).
Пол играет важную роль в общем количестве воды, которое есть у человека. В целом у мужчин процент воды на фунт выше (58%), чем у женщин (49%). Уже сам по себе этот факт позволяет сделать вывод о том, что мужчинам требуется больше алкоголя, чем женщинам, чтобы достичь того же уровня BAC. Кроме того, мужчины в среднем тяжелее женщин. Чем больше воды у человека, тем больше алкоголя требуется для достижения того же соотношения алкоголь: кровь или уровня BAC. Кроме того, исследования показали, что метаболизм алкоголя у женщин отличается от метаболизма мужчин из-за таких биохимических факторов, как разные уровни ацетальдегиддегидрогеназы (фермента, расщепляющего алкоголь) и воздействия оральных контрацептивов.[3]
См. Также
Список литературы
- ↑ Эффекты алкоголя от Технологического института Вирджинии
- ↑ Таблица стандартных напитков от Технологического института Вирджинии
- ↑ BAC Charts от Технологического института Вирджинии
- ↑ Информация взята из Руководства по калибратору Alcotest 7410 GLC. Последнее изменение: октябрь 2000 г., стр. 3A-6.
- ↑ В размере от 0,05% до 0,08% водители могут быть оштрафованы на 135 евро и лишены лицензии на шесть баллов. При превышении 0,08% наказание будет более суровым с возможным лишением свободы на срок до двух лет, крупными штрафами и приостановлением действия лицензии.http://www.securiteroutiere.gouv.fr/infos-ref/regles/l-alcool-au-volant.html (на французском языке)
- ↑ Это в соответствии с разделом 185 Закона об автомобилях 1988 года. За первое нарушение наказанием является тюремное заключение сроком на 6 месяцев и / или штраф в размере 2000 индийских рупий (INR). Если второе преступление совершено в течение трех лет, наказание составляет 2 года и / или штраф в размере 3000 индийских рупий (INR). Пункт о 30 мг / дл был добавлен поправкой в 1994 году. Он вступил в силу с 14 ноября 1994 года.
- ↑ Кроме того, в большинстве юрисдикций полиция и Королевская канадская конная полиция имеют право временно приостанавливать действие водительских прав, если они проходят тестирование на более низких уровнях.
- ↑ Водители младше 21 года (возраст употребления алкоголя в Америке), однако, должны соблюдать более строгие стандарты в соответствии с законами о нулевой терпимости. Эти законы, принятые в различных формах во всех штатах, требуют для водителя гораздо более низких уровней BAC для целей уголовного преследования и / или приостановления действия лицензии, обычно от 0,01% до 0,05%. Во многих штатах есть законодательные нормы, регулирующие вождение в состоянии «под воздействием» интоксиканта, и другой закон о вождении, превышающем допустимую концентрацию алкоголя в крови.
- ↑ http: // caselaw.lp.findlaw.com/casecode/uscodes/18/parts/i/chapters/17a/sections/section_343.html
- Handy Science Answer Book . Питтсбург: Библиотека Карнеги, 1997.
- Тейлор, Л. Защита от вождения в нетрезвом виде , 6-е издание. Нью-Йорк: Закон и бизнес Аспена, 2006. .
- Перхэм, Н. Р., Мур, С. К., Шеперд, Дж. П. и Кьюзенс, Б. (2007). Выявление пьянства в ночном хозяйстве. Наркомания, 102 (3), 377-380
Внешние ссылки
de: Blutalkoholkonzentration мл: രക്തത്തിലെ മദ്യാംശം нет: Алкогольпромилль
Шаблон: WSВыражение Концентрации растворов
В полном описании раствора указывается, что такое растворенное вещество и сколько растворенного вещества растворено в данном количестве растворителя или раствора.Количественное соотношение между растворенным веществом и растворителем — это концентрация решения. Эта концентрация может быть выражена с использованием нескольких различных методов, как обсуждается ниже.
A. Массовая концентрация
Концентрация раствора может быть выражена как масса растворенного вещества в данном количестве раствора, как в следующих утверждениях: Северная часть Тихого океана содержит 35,9 г соли на каждые 1000 г морской воды. В северной части Атлантического океана концентрация соли выше, 37.9 г соли / 1000 г морской воды.
Б. Концентрация в процентах
Концентрация раствора часто выражается как процентная концентрация по массе или объемный процент растворенного вещества в растворе. Массовый процент рассчитывается от массы растворенного вещества в данной массе раствора. 5% -ный водный раствор хлорида натрия содержит 5 г хлорида натрия и 95 г воды на каждые 100 г раствора.Массовый процент = масса растворенного вещества
масса раствораХ 100% Пример:
Сколько граммов глюкозы и воды в 500 г 5.3% раствор глюкозы по массеРешение
Мы знаем, что 5,3% раствора — глюкоза:
Остаток 500 г — вода:
Если и растворенное вещество, и растворитель являются жидкостями, концентрация может быть выражена в процентах по объему. И этиловый спирт, и вода — жидкости; концентрация водно-спиртовых растворов часто указывается в процентах по объему.Например, 95% раствор этилового спирта содержит 95 мл этилового спирта на каждые 100 мл решение.
Объемные проценты = объем растворенного вещества
объем раствораХ 100% Пример:
Медицинский спирт представляет собой водный раствор, содержащий 70% изопропилового спирта. по объему.Как приготовить 250 мл медицинского спирта из чистого изопропилового спирта? алкоголь?Решение
Мы знаем, что 70% объема составляет изопропиловый спирт:
Для приготовления раствора достаточно воды добавляют к 175 мл изопропилового спирта. для образования 250 мл раствора .:
Поскольку плотность жидкости незначительно меняется при изменении температуры, концентрация, указанная в процентах по массе, является точной в более широком диапазоне температур чем концентрация, указанная в объемных процентах.Иногда сочетание массы и объема используется для выражения концентрации — масса растворенного вещества растворяется в каждом 100 мл раствора. Используя этот метод, 5% (вес / объем) раствор хлорида натрия содержит 5 г хлорида натрия на каждые 100 мл раствора.
C. Концентрация в частях на миллион (ppm) и частей на миллиард (ppb) термины (ppm) и части на миллиард (ppb) встречаются все чаще и чаще поскольку мы узнаем о влиянии веществ, присутствующих в следовых количествах в вода и воздух, и поскольку мы разрабатываем инструменты, достаточно чувствительные, чтобы обнаруживать вещества присутствует в таких низких концентрациях.При обсуждении массы части на миллион означают концентрация в граммах на 10 6 граммов или микрограммах на грамм. В при обсуждении объема части на миллион могут означать миллилитры на кубический метр, или смешанное обозначение миллиграммов на кубический метр. Для частей на миллиард, общая тенденция заключается в использовании микрограммов на литр при обсуждении загрязнители воды, микрограммы на кубический метр для воздуха и микрограммы на килограмм для почвенных концентраций.
D. Концентрация в молях
Концентрация раствора может быть указана как молярность (M) — количество молей растворенного вещества на литр раствора или количество миллимолей. (ммоль) (1 миллимоль = 10 -3 моль) на миллилитр раствора.Молярность (M) = моль растворенного вещества
объем (литр) раствора= миллимолей растворенного вещества
миллилитра раствора6 М (скажем, «шестимолярный») раствор соляной кислоты содержит 6 моль соляной кислоты в 1 л раствора.
Молярность раствора дает соотношение между молями растворенного вещества и объемом раствора. Его можно использовать в качестве коэффициента преобразования между этими двумя единицами в расчетах, связанных с решениями. В качестве коэффициента преобразования его можно использовать двумя способами:
- Моль / объем (л) указывает количество молей в одном литре раствора. Этот коэффициент преобразования используется при вычислении количества молей растворенного вещества в данном объеме раствора.
- Объем (л) / моль означает, что один литр содержит некоторое количество молей раствора.Этот коэффициент преобразования используется для расчета объема раствора, содержащего заданное количество растворенного вещества.
Пример:
Сколько молей соляной кислоты содержится в 200 мл 0,15 М HCl?Решение
Разыскивается:
? моль HCl
Учитывая
200 мл 0,15 М HCl
Коэффициенты пересчета
Уравнение
Ответ
0.30 моль HCl
Обратите внимание, что каждый раз, когда указывается объем раствора, концентрация решения дано. Эта форма может показаться запутанной, но без этого отмечая, легко забыть, о каком решении вы говорите.
Пример:
Какая масса гидроксида натрия (NaOH) необходима для приготовления 100 мл 0,125 М гидроксида натрия?Решение
Разыскивается:
? г NaOH
Учитывая
100 мл 0.125 М NaOH
Коэффициенты пересчета
1 л 0,125 М NaOH содержит 0,125 моль NaOH, то есть
Уравнение
Ответ
0,500 г NaOH
Пример:
Какой объем 3,25 М серной кислоты нужен для приготовления 0.500 л 0,130 M H 2 SO 4 ?Решение
Мы должны приготовить 0,500 л 0,130 М h3SO4, добавив некоторое количество воды. до 3,25 М h3SO4. Моли серной кислоты в финале (более разбавленный) раствор будет таким же, как и в молях серной кислоты в порции более концентрированного раствора. Мы можем рассчитать моль серной кислоты в конечном разбавленном растворе:
Этот ответ дает необходимое количество молей кислоты.Мы можем рассчитать объем 3,25 M H 2 SO 4 , который будет содержать 0,065 моль H 2 SO 4 .
Этот ответ дает объем концентрированной кислоты, которая содержит моли. кислоты, необходимой для разбавленного раствора. Это объем 3,25 M H 2 SO 4 будет растворен в 480 мл (500 мл — 20 мл) воды, чтобы приготовить 0,500 л. 0,130 M H 2 SO 4 .Эта проблема изображена на фигура.
Пример:
В каком объеме 6,39 М хлорида натрия содержится 51,2 ммоль хлорида натрия?Решение
Разыскивается
? мл 6,39 М NaClУчитывая
51,2 ммоль NaClКоэффициенты пересчета
1 л из 6.39 M NaCl содержит 6,39 моль NaCl
1 мл 6,39 М NaCl содержит 6,39 ммоль NaClУравнение
Ответ
8,01 мл 6,39 М NaClПример:
Как приготовить 75,0 мл 0,96 М серной кислоты из 18 М кислоты?Решение
Мы должны приготовить 75,0 мл 0,96 М серной кислоты, разбавив 18 М серной кислоты. кислота с водой.Мы можем рассчитать миллимоли серной кислоты в окончательное решение:
Можно рассчитать объем 18 м? ммоль H 2 SO 4 который будет содержать 72 ммоль H 2 SO 4 :
Раствор готовят путем добавления 4,0 мл 18 M H 2 SO 4 примерно до 50 мл воды, а затем разбавьте этот раствор ровно до 75,0 мл.
Таблица 11.3 перечислено несколько наиболее часто используемых способов выражения концентраций.
ТАБЛИЦА 11.3 Общие единицы концентрации Раствор Растворитель Решение Комментарии Весовые проценты ? г + ? г 100 г точный, независимо от температуры Объемные проценты ? мл + ? мл 100 мл используется, когда растворенное вещество является жидким; концентрация незначительно меняется в зависимости от температуры Процент, вес / объем ? г + 100 мл используется, когда растворенное вещество является жидким; концентрация незначительно меняется в зависимости от температуры Молярность (M) моль 1 литр } используется в химических расчетах Миллимоль / литр 10 -3 моль 1 литр Миллимоль / миллилитр 10 -3 моль 10 -3 литр частей на миллион (ppm) мг кг } используется в экологических исследованиях Частей на миллиард (ppb) мкг кг Определение содержания алкоголя в алкогольных напитках с помощью настольного ЯМР-спектрометра 45 МГц.
Спирт или этанол считаются наиболее широко используемыми рекреационными наркотиками во всем мире, и их производство, потребление и продажа строго регулируются законодательством.Содержание алкоголя в алкогольных напитках (вино, пиво и крепкие спиртные напитки) составляет около 3–50% об. / Об. Аналитические методы определения содержания алкоголя должны быть надежными, точными и точными. В этом исследовании количество этанола в нескольких алкогольных напитках определялось с помощью низкопольного спектрометра ЯМР (ядерного магнитного резонанса) с частотой 45 МГц. Для количественного определения этанола использовались аналитические методы внутреннего стандарта и добавления стандарта. Для обоих методов в качестве внутреннего стандарта использовали уксусную кислоту или ацетонитрил для количественного определения содержания спирта с использованием площади пика, соответствующей пикам метила этанола, уксусной кислоты или ацетонитрила.Результаты показали, что метод внутреннего стандарта дал значения процентного содержания спирта, которые находятся в близком соответствии с указанной меткой, что подтверждено обработкой образцов в высокопольном ЯМР-спектрометре с частотой 400 МГц с использованием уксусной кислоты в качестве внутреннего стандарта. Это исследование демонстрирует полезность настольного ЯМР-спектрометра, который может предоставить альтернативный метод анализа процентного содержания алкоголя в алкогольной продукции.
1. Введение
Этанол, обычно называемый этиловым спиртом, является основным спиртовым компонентом вина, полученного путем ферментации сахаров дрожжами.Виноделие — это жестко контролируемый процесс, и конечный товарный продукт подвергается строгим нормам в отношении содержания алкоголя, кислотности, количества диоксида серы, содержания сахара, качества винограда и количества консервантов.
Несколько методов количественного определения содержания алкоголя в вине для обеспечения высочайшего качества основаны на химическом (окисление дихроматом), физическом (пикнометрия, денситометрия, рефрактометрия и гидрометрия), хроматографическом и спектрометрическом анализах.Международная организация винограда и вина (OIV) создала сборник официальных методов тестирования для анализа вин и сусла, которым должны следовать секторы виноградарства, чтобы соответствовать международным стандартам во всем мире. Спектроскопические методы, такие как инфракрасный (ИК), ЯМР и масс-спектрометрия, предлагают альтернативные методы, отличные от традиционных химических испытаний и хроматографических методов, таких как высокоэффективная жидкостная хроматография (ВЭЖХ) и газовая хроматография (ГХ) [1–16]. Недавно рамановская спектроскопия была исследована для количественной оценки концентрации этанола в алкогольных напитках [17].Чтобы соответствовать международным энологическим стандартам и сохранить высокое качество продукции, методы определения содержания алкоголя должны быть надежными для измерения этого очень важного параметра [9]. Дополнительным преимуществом было бы, если бы реализованный метод был официально признан, но недорог и менее подвержен человеческим ошибкам.
Спектроскопия ядерного магнитного резонанса (ЯМР), неразрушающий неинвазивный метод, который обеспечивает прямую связь между измеренными спектрами и химической структурой, является основным стандартным и рутинным методом определения характеристик молекулярной структуры.Способность ЯМР для количественного определения (qNMR) одновременно обнаруживать большое количество соединений в сложной смеси без разделения оказывается выгодным методом анализа природных продуктов [18, 19], включая пищевые продукты, фруктовые соки или алкогольные напитки. напитки [20–23]. В частности, методики ЯМР 1 H применялись для определения химических компонентов (фенольных смол, сахаров и органических кислот) и для измерения количества алкоголя для проверки качества вина [24–27].ЯМР-анализ применялся даже в полностью неповрежденных винных бутылках, чтобы сохранить целостность этого ценного товара [28, 29].
Целью этого исследования было изучение использования низкопольного ЯМР-спектрометра 45 МГц для определения содержания спирта в некоторых алкогольных продуктах. Настольный ЯМР-спектрометр использовался в обучении лабораторным методам органической химии [30, 31] и набирает популярность благодаря простоте и рентабельности его использования, включая приложения для получения изображений in vivo [32, 33], по сравнению с высокопольными приборами ЯМР.
2. Материалы и методы
2.1. Материалы
Имеющиеся в продаже алкогольные напитки были получены от местных коммерческих поставщиков и проанализированы на содержание алкоголя. Было использовано четырнадцать различных образцов алкоголя: банановый ликер (KY, США), ром Black Magic (KY, США), водка Fleischmann’s (Лос-Анджелес, Калифорния, США), водка Smirnoff (Norwalk, CT, США), водка Stolichnaya (Латвия), Three Водка с оливками (Рочестер, Нью-Йорк), пивной ликер доктора МакГилликадди (Висконсин, США), красное вино Мерло (Модесто, Калифорния), ром Cruzan Key Lime (Иллинойс, США), Пино Нуар (Модесто, Калифорния, США), канадский ледяное вино (Ниагара на озере, Онтарио, Канада), Tour de Soleil Rosé (Кот-де-Гасконь, Франция), Beringer White Zinfandel (Напа, Калифорния, США) и белое вино Москато (Модесто, Калифорния, США).Абсолютный этанол (степень доказательства 200), используемый в качестве калибровочного стандарта, был получен от Mallinckrodt Chemicals (Сент-Луис, Миссури, США). Уксусная кислота и ацетонитрил были получены от Sigma Aldrich (Сент-Луис, Миссури, США). Дейтерированная вода (D 2 O, 99,9% D) была приобретена в Cambridge Isotope Laboratories (Тьюксбери, Массачусетс, США).
2.2. Приготовление образца Образцы ЯМР
для метода внутреннего стандарта были приготовлены путем измерения 900 мкл л спиртовых образцов и 100 мкл л ледяной уксусной кислоты в небольшом закрытом флаконе объемом 3 мл для общего объема 1 мл.Было приготовлено пять различных смесей. Растворы хорошо перемешивали и сразу же использовали для анализа в спектрометре ЯМР 45 МГц. Для сравнения были приготовлены образцы ЯМР для спектрометра ЯМР 400 МГц путем помещения 100 мкл л смеси образцов уксусной кислоты и спирта в 5-миллиметровую пробирку для ЯМР в сочетании с 600 мкл л D 2 O. Дополнительно, ацетонитрил также использовался в качестве внутреннего стандарта вместо уксусной кислоты. Образцы ЯМР для калибровочной кривой были приготовлены путем смешивания 10–90% абсолютного этанола и фиксированного количества уксусной кислоты (10%) в качестве внутреннего стандарта для общего объема 1 мл в воде milliQ.Образцы для стандартного метода добавления были приготовлены с абсолютной концентрацией этанола в диапазоне от 0 до 50% объема / объема, добавляемого в смесь. Приготовление шести образцов для стандартного метода добавления показано в таблице 1.
% EtOH EtOH (мл) Образец (мл) Внутренний стандарт (мл) H 2 O (мл) Общий объем (мл) 0 0 0.5 0,1 1,4 2,0 10 0,2 0,5 0,1 1,2 2,0 20 0,4 908 1,030 0,6 0,5 0,1 0,8 2,0 40 0,8 0,5 0,1 0,6 2.0 50 1 0,5 0,1 0,4 2,0 2.3.
1 H ЯМР-спектроскопияОколо 200–300 мкл л смеси спирта и уксусной кислоты вводили во входное отверстие прибора для ЯМР 45 МГц. Петля для образца вмещает около 20 мкл л жидкости. Вводится проба, примерно в десять раз превышающая объем петли для отбора проб, чтобы гарантировать, что анализируемая проба находится внутри петли, а капли жидкости стекают из выпускного отверстия.Спектры ЯМР 1 H получали на спектрометре ЯМР picoSpin 45 МГц, оборудованном фиксированным магнитом. Перед спектральной съемкой использовалась отливка на воде. Одномерные одноимпульсные спектры 1 H ЯМР, генерируемые как экспоненциально затухающая синусоида или спад свободной индукции (FID), были получены с использованием одноимпульсной последовательности, доступной в библиотеке сценариев импульсов picoSpin. ПИД собирали при 298 К с использованием задержки релаксации 8 с, ширины импульса 90 ° (43 мкм с) и 16 сканирований.Спектры ЯМР 1 H также получали на спектрометре ЯМР Bruker Avance 400 МГц, оборудованном автосэмплером. Одномерные одноимпульсные спектры ЯМР 1 H были получены с использованием одноимпульсной последовательности в библиотеке импульсных последовательностей Bruker. ПИД собирали при 298 К с использованием задержки релаксации 1 с, ширины импульса 90 ° (14,9 мкм с) и 16 сканирований. Оба FID были аподизированы экспоненциальным умножением до преобразования Фурье. Химические сдвиги ( δ ) даны в м.д. относительно уксусной кислоты (или ацетонитрила), установленной на 2.04 промилле. Обработку проводили с использованием программного обеспечения обработки данных ACD / Labs NMR Processor Version 12.01 и TopSpin 2.1.6 для приборов ЯМР 45 и 400 МГц соответственно.
3. Результаты и обсуждение
Спектр ЯМР представляет собой график зависимости приложенной радиочастоты от поглощения, а сигнал ЯМР называется резонансом, выраженным как химический сдвиг в ppm, который не зависит от частоты спектрометра [34] . Важные особенности спектра ЯМР, которые предоставляют информацию, относящуюся к структуре молекулы, включают химический сдвиг, множественность, интеграцию пика и константу взаимодействия.Химический сдвиг зависит от наблюдаемого окружения ядра (такого как водород или H). Водороды вблизи электроотрицательных атомов (O, N и галогенов), испытывающих пониженную электронную плотность, будут деэкранированы и будут резонировать в слабом поле или при более высоких ppm. Кроме того, протоны в ароматических соединениях (бензол) и алкенах (двойные связи) смещены в слабое поле вследствие индуцированного магнитного поля из-за циркулирующих электронов или анизотропных эффектов. Множественность или спин-спиновое расщепление относится к взаимодействию ядра с соседними ядрами или водорода с соседними атомами водорода и может быть оценено эмпирически по правилу (), в котором резонансный пик разбивается на компоненты (), где относится к количество эквивалентных атомов водорода () на соседнем атоме (ах).Наблюдаемая множественность, которая зависит от числа соседних атомов водорода, приведет к появлению структур расщепления, обозначенных как синглет (без смежного водорода), дублет (1 смежный H), триплет (2 смежных H), квартет (3 смежных H) и т. Д. вперед. Интеграция относится к площади под пиком (ами) или мультиплетами, которая является мерой количества атомов водорода в этом конкретном резонансе или химическом сдвиге. Константа (или значение) связи является мерой взаимодействия или связи соседних ядер, так что атомы водорода, разделенные тремя связями, будут связаны друг с другом и будут иметь одинаковую константу или значение связи.Для этанола (CH 3 CH 2 OH) существует три уникальных атома водорода, которые проявляются в виде трех отдельных сигналов ЯМР: CH 3 (метил) при 1,18 ppm, CH 2 (метилен) при 3,64 ppm, и ОН (гидроксил) при 4,80, который перекрывается с пиком воды. Картина расщепления для этанола будет триплетной для CH 3 , квартетной для CH 2 и синглетной для OH с коэффициентом интеграции пиков 3: 2: 1, соответствующим CH 3 , CH 2 и OH, соответственно.Гидроксильный протон будет проявляться в виде широкого синглета как на спектрометрах 45, так и на 400 МГц из-за присутствия воды и остаточных атомов водорода в дейтерированных растворителях. Для абсолютного или сверхчистого безводного этанола расщепление пика ОН наблюдается в спектрометре ЯМР 45 МГц, используемом для этого исследования [35], поскольку жидкий образец обрабатывается в чистом виде и не растворяется в дейтерированном растворителе, что может вызвать расширение гидроксильной группы. в образце за счет протонного обмена. значение для связи CH 3 и CH 2 составляет ~ 6 Гц.
На рис. 1 показаны ЯМР-спектры спиртовых образцов, полученные с помощью настольного спектрометра 45 МГц и ЯМР-спектрометра 400 МГц. Триплет, отнесенный к метильной (CH 3 ) группе при 1,18 м.д., был пиком, используемым для количественного определения по формуле, показанной в (1), где количество этанола, который является основным компонентом, рассчитывается непосредственно из спектра ЯМР. . Это основано на стандартных аналитических процедурах определения концентраций аналитов [13–33, 36]. Синглет метильного пика при 2.Для калибровки использовали 04 ч / млн, соответствующие уксусной кислоте или ацетонитрилу, и в качестве эталона устанавливали 3 для интегрирования пиков для определения содержания спирта в образцах. Пик метилена (CH 2 ) имеет тенденцию иметь перекрывающийся пик со спиртовым продуктом, вероятно, из-за молекул сахара и других растворенных веществ и, следовательно, не используется для анализа. Определение содержания алкоголя в алкогольных напитках показано следующим образом: где — количество атомов водорода; это объем.
Определение процентного содержания алкоголя в образце представляло собой простой расчет, основанный на среднем значении 5 различных образцов приготовления одного и того же алкогольного продукта.Уксусная кислота используется в качестве внутреннего стандарта для количественного определения путем интегрирования пиков [16, 28], поскольку она легко доступна, дешева, стабильна, нелетучая и растворима в водных этанольных растворах. Контрольный сигнал для метильной группы при 2,04 м.д. является синглетом и сильно отделен от пиков этанола. Ацетонитрил также использовали в качестве внутреннего стандарта, используя пик метила также при 2,04 м.д. Кроме того, по одному образцу каждого спиртового продукта обрабатывали на ЯМР-спектрометре 400 МГц (см. Рисунок 1), и результаты, полученные для настольного ЯМР, сопоставимы.
Очевидно, что для 400 МГц наблюдается более высокое разрешение, чем для 45 МГц, как показано на рисунке 1. Подготовка образцов для приборов с низкой и высокой напряженностью поля различается. Для настольного прибора требуется меньше пробоподготовки, в то время как для высокопольного ЯМР-прибора смесь спирта и уксусной кислоты растворяется в дейтерированной воде (D 2 O) для фиксации. Густые и молочные алкогольные продукты, такие как Tequila Rose и Chiata Rum, не могут быть определены с помощью настольного ЯМР 45 из-за трудностей с введением образцов.
Таблица 2 суммирует результаты, полученные для определения содержания этанола в нескольких имеющихся в продаже алкогольных напитках с использованием приборов как на 45, так и на 400 МГц. Методики, используемые для определения содержания алкоголя, включают использование внутреннего стандарта и метода добавления стандартов. Использование внутреннего стандарта, в котором уксусная кислота или ацетонитрил добавлялись непосредственно к образцу, увеличивает надежность и точность расчетов для определений, используемых для обоих инструментов.Стандартный метод добавления, показанный на рисунке 2, включает добавление известных количеств этанола для корректировки матричных эффектов. Оба метода (внутренний стандарт или метод добавления стандартов) требуют использования внутреннего стандарта для калибровки для интеграции пиков. Метод добавления внутреннего стандарта требует меньшего количества пробоподготовки и будет предпочтительным методом выбора при определении значительного количества проб. Кривая линейности для стандартных концентраций в диапазоне от 10 до 90% этанола в воде с уксусной кислотой в качестве эталона показана на рисунке 3 для спектрометра ЯМР 1 H с частотой 45 МГц.Метод внешнего стандарта с использованием калибровочной кривой, такой как показанная на рисунке 3, с использованием уксусной кислоты для интегрирования пиков, привел к ошибочным расчетам содержания спирта и не использовался в данном исследовании. Окончательное определение содержания спирта было в первую очередь основано на интеграции пиков метильных (CH 3 ) пиков, относящихся к уксусной кислоте или ацетонитрилу, с использованием (1), поскольку наблюдалось, что эта спектральная область ЯМР значительно меньше зависит от перекрытия, вызванного другими компонентами. в образце по сравнению с метиленовой (CH 2 ) областью, где наблюдались другие пики (см. рисунок 1).Ссылка или стандарт, добавленный внутри, будут необходимы всегда для количественного определения количества алкоголя. Уксусная кислота и ацетонитрил были выбраны в качестве внутренних стандартов из-за стоимости, сходства молекулярной структуры с этанолом и простоты приготовления, поскольку это жидкие стандарты по сравнению с натриевой солью 3- (триметил-силил) -1-пропансульфоновой кислоты (DSS) или (CH 3 ) 3 Si (CD 2 ) 2 CO 2 Na, 3-триметилсилилпропионат-2,2,3,3-d натрия 4 (TMSP), оба которые являются твердыми телами.Не было обнаружено значительного количества уксусной кислоты в алкогольных напитках, которые использовались в этом исследовании, как показано на рисунках 4 (a) и 4 (c), на которых алкогольные напитки были обработаны как чистые образцы на спектрометре 45 МГц и подтверждены, когда то же самое. образцы (растворенные в D 2 O) обрабатывали в приборе 400 МГц (см. рисунки 4 (b) и 4 (d)). Если бы уксусная кислота присутствовала в алкогольном напитке в значительном количестве, то количество изначально присутствующей уксусной кислоты можно было бы рассчитать, проанализировав два образца: один со стандартом уксусной кислоты известного количества, а другой без стандарта уксусной кислоты.Площадь пика для образца с добавленным стандартом уксусной кислоты будет больше, чем без него. Следовательно, количество присутствующего этанола может быть соответственно скорректировано.
Алкогольные напитки % спирта
на этикетке% спирта
400 МГц
HOAc IS% спирта IS
45 МГц%
ACC 45 IS% спирта
45 МГц
HOAc SA% спирта
45 МГц
ACN SAБанановый ликер 49.5 46,80 49,03 0,24 53,69 0,19 54,56 0,46 56,46 0,58 Ром Блэк Мэджик 47 46,07 48,81 908,19 46,07 48,81 90,81 0,9 Водка Флейшманна 40 37,07 39,15 1,13 40,04 2,07 44,56 0,28 44,62 1,42 Водка Smirnoff 83 43,39 0,15 42,21 0,25 42,05 0,78 44,50 0,49 Водка «Столичная» 37,5 37,33 37,84 0,9014 37,84 0,9014 908 Водка с оливками30 28,05 33,54 0,26 32,39 0,62 30,04 0,59 34,05 0,42 Пивной ликер Dr. McGillicuddy’s 21 908.15 20,51 1,10 21,47 0,60 22,26 0,35 22,25 0,56 Крузан Ки Лайм ром 21 20,50 26,33 0,21 814 26,33 0,21 814 20,33 Красное вино Мерло 13 11,30 13,36 0,09 13,41 0,15 15,89 0,32 15,32 0,31 Пино Нуар 11.5 10,13 11,47 0,07 11,25 0,11 10,22 0,37 11,58 0,39 Канадское ледяное вино 11 10,23 11,81414 0,10 11 9004 11,8147 0,10 908Tour de Soleil Rosé 11 11,50 9,94 0,28 11,51 0,43 13,51 0,20 14,49 0,76 Bering14 908andel Zinfandel569,26 0,32 13,10 0,24 10,92 0,21 13,13 0,22 Вино Москато белое 9 7,69 9,09 0,28 9,09 0,28 9,609 0,09 0,09 0,09
Чтобы получить точное интегрирование пиков для количественного эксперимента ЯМР, обычно используется приблизительно значение задержки релаксации [19].относится к постоянной времени или времени релаксации для ядра, чтобы полностью расслабиться между импульсами и вернуться к равновесию. Каждое ядро в молекуле будет иметь разные значения из-за разной магнитной среды. Для спектрометра 45 МГц использовалась задержка релаксации 8 секунд. Однако 1-секундная задержка релаксации использовалась для сокращения времени работы для прибора FT с частотой 400 МГц, поскольку при изменении значения с 1-секундной на 8-10-секундную задержку наблюдалась незначительная разница около 0,1–0,3%.
Основываясь на результатах этого исследования, метод внутреннего стандарта, выполненный в низкопольном настольном ЯМР-спектрометре 45 МГц, дал уровни процентного содержания спирта, которые более сопоставимы с меткой, чем метод стандартного добавления, и поэтому был использован метод для сравнения с высокопольный ЯМР-спектрометр 400 МГц. Результаты, полученные для спектрометра 45 МГц и 400 МГц, немного различаются, скорее всего, из-за различий в подготовке образца. Образцы для частоты 400 МГц представляли собой 100 аликвот мкл л, полученных из образцов, приготовленных для частоты 45 МГц, и аликвоты, разбавленные дейтерированной водой.Несоответствие в точных измерениях объема могло внести эту разницу.
Самым важным преимуществом использования настольного ЯМР-спектрометра 45 МГц по сравнению с прибором с сильным полем является стоимость. ЯМР с фиксированным магнитом в слабом поле по сравнению со сверхпроводящим высокопольным спектрометром требует меньшего обслуживания, поскольку не требуются криогены, что позволяет избежать дополнительных задач для персонала по управлению прибором. Пробирки для ЯМР и дейтерированные растворители, необходимые для стабилизации поля / частоты для высокополевых приборов [37], не являются необходимыми, что снижает дополнительные расходы, связанные с анализом образцов.
4. Заключение
Настольная технология ЯМР обеспечивает экономичное и низкое техническое обслуживание оборудования по сравнению с приборами ЯМР с сильным полем и может быть многообещающим методом в будущем для винодельческой промышленности для анализа содержания алкоголя для подтверждения качества вина.
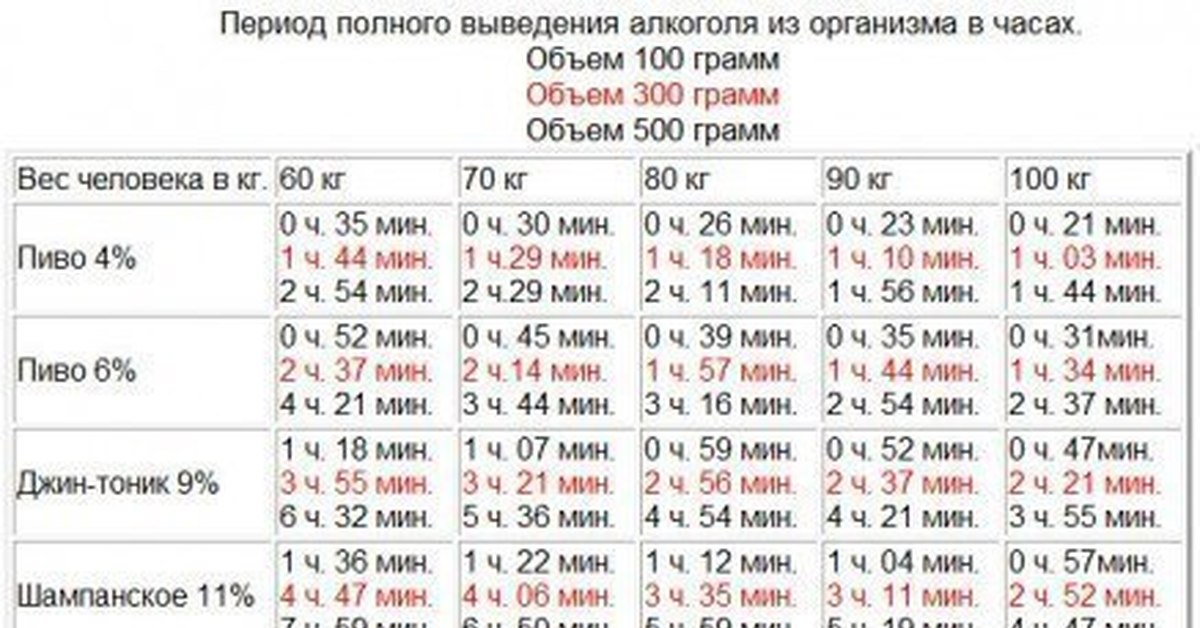
 Здесь необходимо вспомнить школьную программу обучения. Напомним, что в организме мужчины содержится 70% жидкости. Следовательно, масса жидкости равна 63 кг.
Здесь необходимо вспомнить школьную программу обучения. Напомним, что в организме мужчины содержится 70% жидкости. Следовательно, масса жидкости равна 63 кг.
